
中考化学 黄金知识点系列 专题10 盐和化肥-人教版初中九年级全册化学试题.doc

永梅****33










亲,该文档总共12页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

中考化学 黄金知识点系列 专题10 盐和化肥-人教版初中九年级全册化学试题.doc
考点十:盐和化肥考试说明了解食盐、纯碱、小苏打、碳酸钙等盐在日常生活中的用途。知道一些常用化肥的名称和作用。初步学会根据某些性质检验和区分一些常见的物质。4.初步学习使用过滤、蒸发的方法对混合物进行分离。聚焦考点☆温习理解考点1常见的盐1:盐的概念、概念:盐是有金属离子(或铵根离子)和酸根离子组成的一类化合物。2:几种常见的盐(食盐、纯碱、小苏打、碳酸钙等盐在日常生活中的用途)物质俗称物理性质用途氯化钠(NaCl)食盐的主要成分白色粉末水溶液有咸味溶解度受温度影响不大(1)作调味品(2)作防腐剂(3

中考化学 黄金知识点系列 专题10 盐和化肥-人教版初中九年级全册化学试题.doc
考点十:盐和化肥考试说明了解食盐、纯碱、小苏打、碳酸钙等盐在日常生活中的用途。知道一些常用化肥的名称和作用。初步学会根据某些性质检验和区分一些常见的物质。4.初步学习使用过滤、蒸发的方法对混合物进行分离。聚焦考点☆温习理解考点1常见的盐1:盐的概念、概念:盐是有金属离子(或铵根离子)和酸根离子组成的一类化合物。2:几种常见的盐(食盐、纯碱、小苏打、碳酸钙等盐在日常生活中的用途)物质俗称物理性质用途氯化钠(NaCl)食盐的主要成分白色粉末,水溶液有咸味,溶解度受温度影响不大(1)作调味品(2)作防腐剂(3)

中考化学考点总动员系列 专题10 盐和化肥-人教版初中九年级全册化学试题.doc
考点十:盐和化肥聚焦考点☆温习理解一:盐的概念、概念:盐是有金属离子(或铵根离子)和酸根离子组成的一类化合物。二:几种常见的盐(食盐、纯碱、小苏打、碳酸钙等盐在日常生活中的用途)物质俗称物理性质用途氯化钠(NaCl)食盐的主要成分白色粉末,水溶液有咸味,溶解度受温度影响不大(1)作调味品(2)作防腐剂(3)消除积雪(降低雪的熔点)(4)农业上用NaCl溶液来选种(5)制生理盐水(0.9%NaCl溶液)Na+维持细胞内外的水分分布,促进细胞内外物质交换Cl-促生盐酸、帮助消化,增进食欲碳酸氢钠(NaHCO3
中考化学知识点专题训练十三 盐和化肥-人教版初中九年级全册化学试题.doc
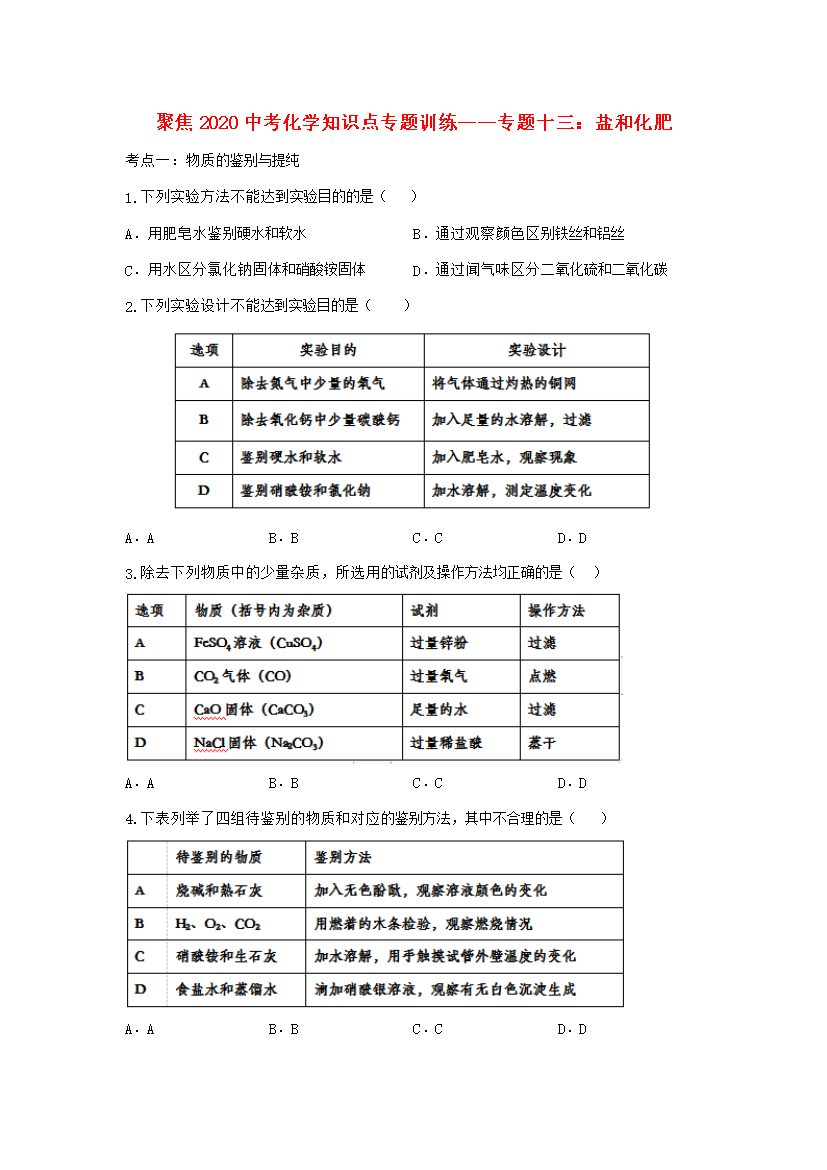
聚焦2020中考化学知识点专题训练——专题十三:盐和化肥考点一:物质的鉴别与提纯1.下列实验方法不能达到实验目的的是()A.用肥皂水鉴别硬水和软水B.通过观察颜色区别铁丝和铝丝C.用水区分氯化钠固体和硝酸铵固体D.通过闻气味区分二氧化硫和二氧化碳2.下列实验设计不能达到实验目的是()A.AB.BC.CD.D3.除去下列物质中的少量杂质所选用的试剂及操作方法均正确的是()A.AB.BC.CD.D4.下表列举了四组待鉴别的物质和对应的鉴别方法其中不合理的是()A.AB.BC.CD.D5.下

中考化学知识点专题训练十三 盐和化肥-人教版初中九年级全册化学试题.doc
聚焦2020中考化学知识点专题训练——专题十三:盐和化肥考点一:物质的鉴别与提纯1.下列实验方法不能达到实验目的的是()A.用肥皂水鉴别硬水和软水B.通过观察颜色区别铁丝和铝丝C.用水区分氯化钠固体和硝酸铵固体D.通过闻气味区分二氧化硫和二氧化碳2.下列实验设计不能达到实验目的是()A.AB.BC.CD.D3.除去下列物质中的少量杂质,所选用的试剂及操作方法均正确的是()A.AB.BC.CD.D4.下表列举了四组待鉴别的物质和对应的鉴别方法,其中不合理的是()A.AB.BC.CD.D5.下列实验方案中,能
