
福建省东桥经济开发区九年级化学《酸和碱》教案.doc

森林****io





在线预览结束,喜欢就下载吧,查找使用更方便
相关资料

福建省东桥经济开发区九年级化学《酸和碱》教案.doc
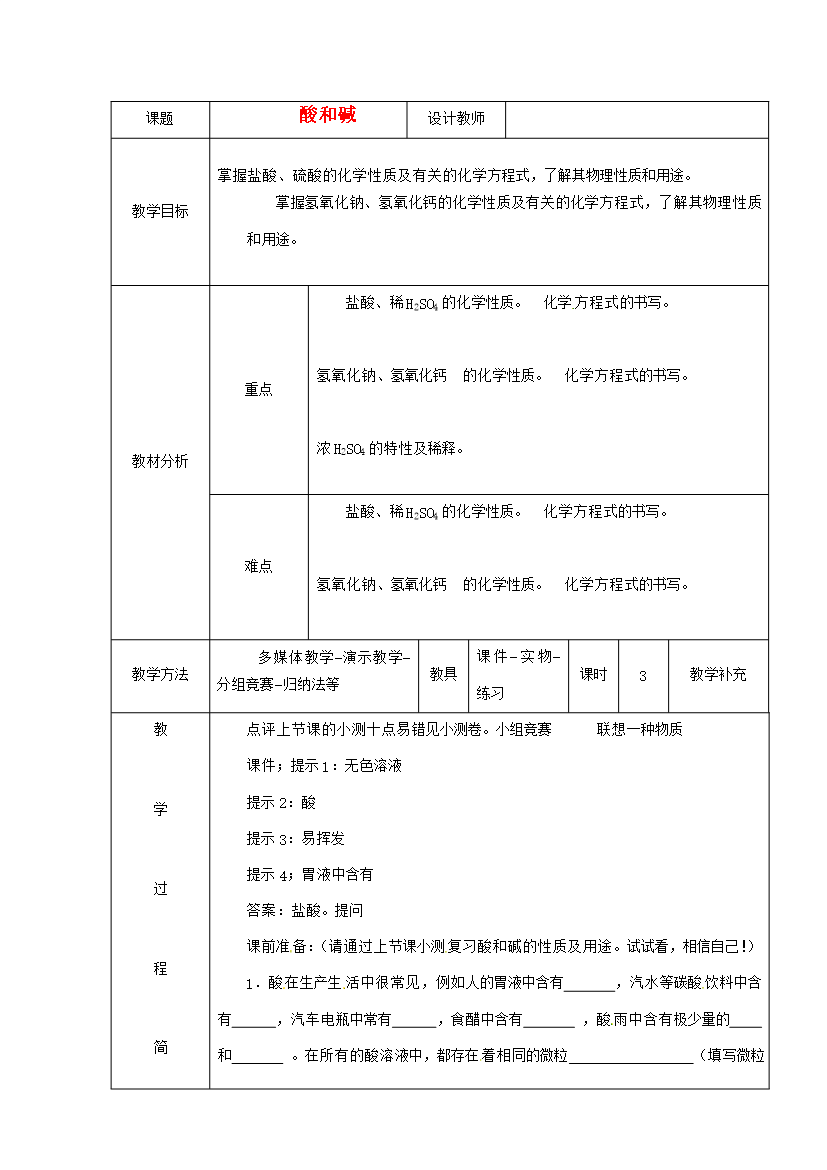
课题酸和碱设计教师教学目标掌握盐酸、硫酸的化学性质及有关的化学方程式,了解其物理性质和用途。掌握氢氧化钠、氢氧化钙的化学性质及有关的化学方程式,了解其物理性质和用途。教材分析重点盐酸、稀H2SO4的化学性质。化学方程式的书写。氢氧化钠、氢氧化钙的化学性质。化学方程式的书写。浓H2SO4的特性及稀释。难点盐酸、稀H2SO4的化学性质。化学方程式的书写。氢氧化钠、氢氧化钙的化学性质。化学方程式的书写。教学方法多媒体教学-演示教学-分组竞赛-归纳法等教具课件-实物-练习课时3教学补充教学过程简记点评上节课的小测
福建省东桥经济开发区九年级化学《酸和碱》教案.doc
课题酸和碱设计教师教学目标掌握盐酸、硫酸的化学性质及有关的化学方程式了解其物理性质和用途。掌握氢氧化钠、氢氧化钙的化学性质及有关的化学方程式了解其物理性质和用途。教材分析重点盐酸、稀H2SO4的化学性质。化学方程式的书写。氢氧化钠、氢氧化钙的化学性质。化学方程式的书写。浓H2SO4的特性及稀释。难点盐酸、稀H2SO4的化学性质。化学方程式的书写。氢氧化钠、氢氧化钙的化学性质。化学方程式的书写。教学方法多媒体教学-演示教学-分组竞赛-归纳法等教具课件-实物-练习课时3教学补充教学过程简记点评

教案-福建-2012_福建省东桥经济开发区九年级化学《酸和碱》教案.rar
1用心爱心专心课题酸和碱设计教师教学目标掌握盐酸、硫酸的化学性质及有关的化学方程式,了解其物理性质和用途。掌握氢氧化钠、氢氧化钙的化学性质及有关的化学方程式,了解其物理性质和用途。教材分析重点盐酸、稀H2SO4的化学性质。化学方程式的书写。氢氧化钠、氢氧化钙的化学性质。化学方程式的书写。浓H2SO4的特性及稀释。难点盐酸、稀H2SO4的化学性质。化学方程式的书写。氢氧化钠、氢氧化钙的化学性质。化学方程式的书写。教学方法多媒体教学-演示教学-分组竞赛-归纳法等教

福建省东桥经济开发区九年级化学《酸和碱》复习课件(2).ppt
酸碱盐de复习九年级化学酸、碱、盐的组成、分类学会归纳2.酸碱盐的组成本章常见化合物写出下列物质的化学式并指出它们各属于哪一类化合物:酸、碱、盐的化学性质4、酸+碱→盐+水4.碱+盐→新盐+新碱盐+金属→新金属+新盐3、金属跟硝酸或浓硫酸起反应时由于硝酸或浓硫酸的氧化性很强一般不生成氢气。且即使活动性排在氢后面的金属也能和硝酸或浓硫酸发生氧化还原反应。4.钾、钙、钠等化学性质极为活泼的金属跟盐溶液反应的情况比较

福建省东桥经济开发区九年级化学《酸和碱》教学课案.doc
课题酸和碱设计教师教学目标掌握盐酸、硫酸的化学性质及有关的化学方程式,了解其物理性质和用途。掌握氢氧化钠、氢氧化钙的化学性质及有关的化学方程式,了解其物理性质和用途。教材分析重点盐酸、稀H2SO4的化学性质。化学方程式的书写。氢氧化钠、氢氧化钙的化学性质。化学方程式的书写。浓H2SO4的特性及稀释。难点盐酸、稀H2SO4的化学性质。化学方程式的书写。氢氧化钠、氢氧化钙的化学性质。化学方程式的书写。教学方法多媒体教学-演示教学-分组竞赛-归纳法等教具课件-实物-练习课时3教学补充教学过程简记点评上节课的小测
