
广东深圳名校中考化学 《水和溶液》复习学习预案 人教版.doc

my****25










亲,该文档总共11页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

广东深圳名校中考化学 《水和溶液》复习学习预案 人教版.doc
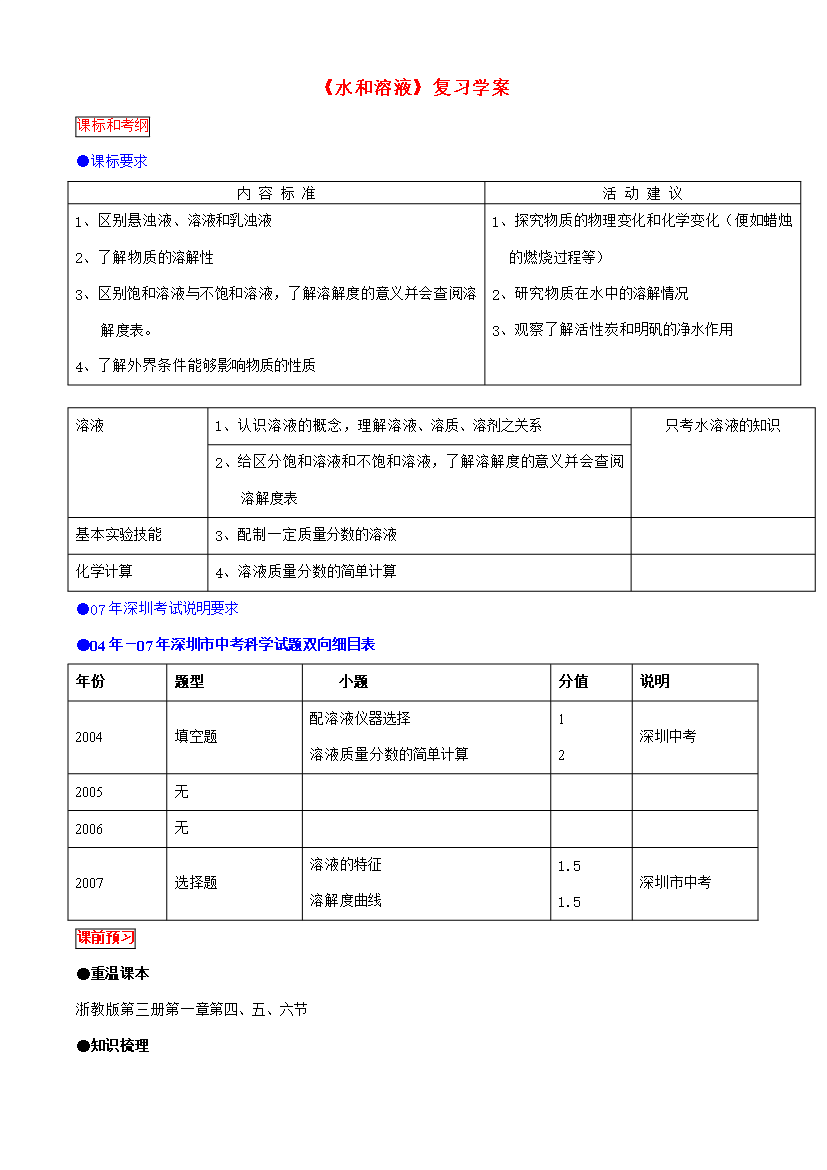
《水和溶液》复习学案课标和考纲●课标要求内容标准活动建议1、区别悬浊液、溶液和乳浊液2、了解物质的溶解性3、区别饱和溶液与不饱和溶液,了解溶解度的意义并会查阅溶解度表。4、了解外界条件能够影响物质的性质1、探究物质的物理变化和化学变化(便如蜡烛的燃烧过程等)2、研究物质在水中的溶解情况3、观察了解活性炭和明矾的净水作用溶液1、认识溶液的概念,理解溶液、溶质、溶剂之关系只考水溶液的知识2、给区分饱和溶液和不饱和溶液,了解溶解度的意义并会查阅溶解度表基本实验技能3、配制一定质量分数的溶液化学计算4、溶液质量分

广东深圳名校中考化学 《水和溶液》复习学案 人教版.doc
《水和溶液》复习学案课标和考纲●课标要求内容标准活动建议1、区别悬浊液、溶液和乳浊液2、了解物质的溶解性3、区别饱和溶液与不饱和溶液,了解溶解度的意义并会查阅溶解度表。4、了解外界条件能够影响物质的性质1、探究物质的物理变化和化学变化(便如蜡烛的燃烧过程等)2、研究物质在水中的溶解情况3、观察了解活性炭和明矾的净水作用溶液1、认识溶液的概念,理解溶液、溶质、溶剂之关系只考水溶液的知识2、给区分饱和溶液和不饱和溶液,了解溶解度的意义并会查阅溶解度表基本实验技能3、配制一定质量分数的溶液化学计算4、溶液质量分
广东深圳名校中考化学 《水和溶液》复习学案 人教版.doc
《水和溶液》复习学案课标和考纲●课标要求内容标准活动建议1、区别悬浊液、溶液和乳浊液2、了解物质的溶解性3、区别饱和溶液与不饱和溶液了解溶解度的意义并会查阅溶解度表。4、了解外界条件能够影响物质的性质1、探究物质的物理变化和化学变化(便如蜡烛的燃烧过程等)2、研究物质在水中的溶解情况3、观察了解活性炭和明矾的净水作用溶液1、认识溶液的概念理解溶液、溶质、溶剂之关系只考水溶液的知识2、给区分饱和溶液和不饱和溶液了解溶解度的意义并会查阅溶解度表基本实验技能3、配制一定质量分数的溶液化学计算4、溶液

广东深圳名校中考化学 《水和溶液》复习学案 人教版.doc
《水和溶液》复习学案课标和考纲●课标要求内容标准活动建议1、区别悬浊液、溶液和乳浊液2、了解物质的溶解性3、区别饱和溶液与不饱和溶液了解溶解度的意义并会查阅溶解度表。4、了解外界条件能够影响物质的性质1、探究物质的物理变化和化学变化(便如蜡烛的燃烧过程等)2、研究物质在水中的溶解情况3、观察了解活性炭和明矾的净水作用溶液1、认识溶液的概念理解溶液、溶质、溶剂之关系只考水溶液的知识2、给区分饱和溶液和不饱和溶液了解溶解度的意义并会查阅溶解度表基本实验技能3、配制一定质量分数的溶液化学计算4、溶液

学案-广东-2010_广东深圳名校中考化学 《水和溶液》复习学案 人教版.rar
《水和溶液》复习学案课标和考纲●课标要求内容标准活动建议1、区别悬浊液、溶液和乳浊液2、了解物质的溶解性3、区别饱和溶液与不饱和溶液,了解溶解度的意义并会查阅溶解度表。4、了解外界条件能够影响物质的性质1、探究物质的物理变化和化学变化(便如蜡烛的燃烧过程等)2、研究物质在水中的溶解情况3、观察了解活性炭和明矾的净水作用溶液1、认识溶液的概念,理解溶液、溶质、溶剂之关系只考水溶液的知识2、给区分饱和溶液和不饱和溶液,了解溶解度的意义并会查阅溶解度表基本实验技能3、配制一定质量分数的溶
