
混合溶液的pH计算ppt课件.ppt

天马****23








亲,该文档总共18页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

混合溶液的pH计算ppt课件.ppt
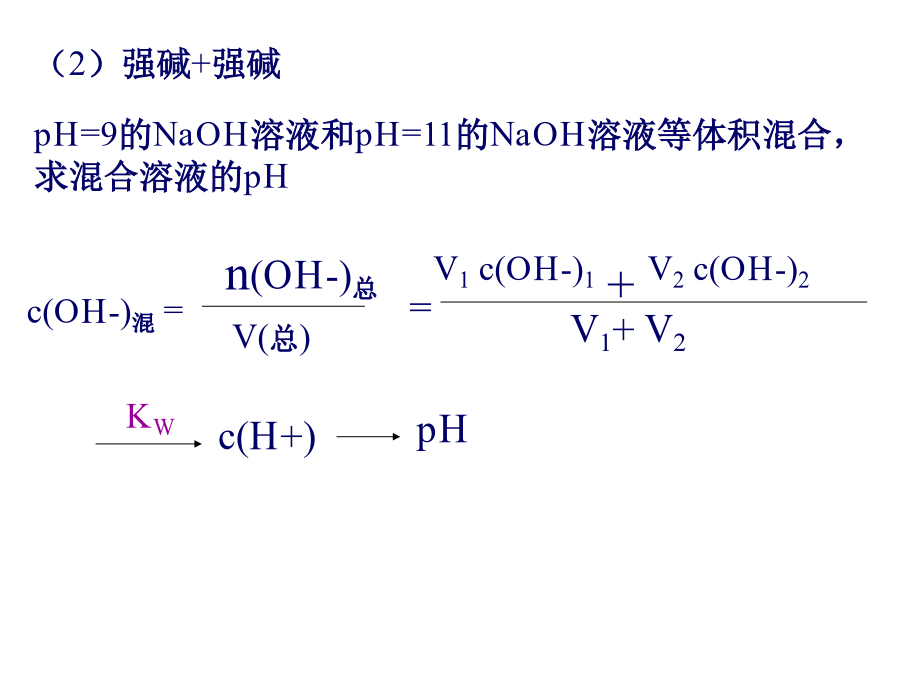
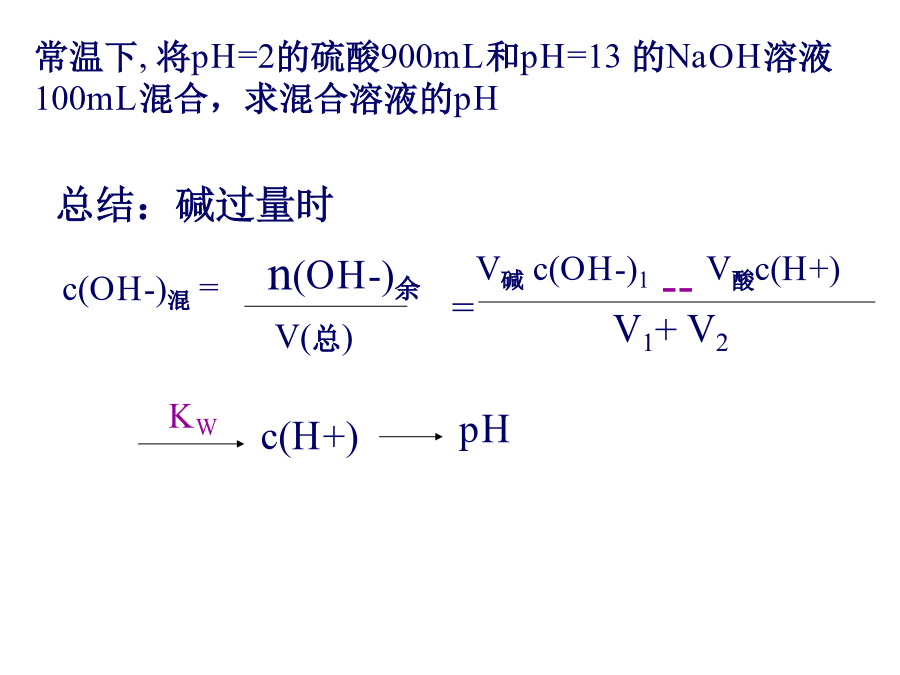
有关混合溶液pH的计算2.混合溶液的pH计算pH=9的NaOH溶液和pH=11的NaOH溶液等体积混合,求混合溶液的pH(3)强酸+强碱常温下,将0.3mol/L的盐酸和0.1mol/L的NaOH溶液各100mL混合,求混合溶液的pH常温下,将pH=2的硫酸900mL和pH=13的NaOH溶液100mL混合,求混合溶液的pH3.有关溶液的稀释pH=1的醋酸和盐酸均加水稀释,使体积为原来的1000倍则判断pH值正误(未给明条件时)不能用pH值等于多少来判断溶液酸、碱性。练习3室温时,下列溶液中碱性最强的是(

混合溶液PH的计算ppt课件.ppt
第三课时混合溶液pH的计算强酸与强酸混合关键:1.抓住氢离子进行计算。2.当相加、减的两个量相差100倍以上时,小的量可忽略。强碱与强碱混合=-lg(2×10-10)1.pH=2的盐酸和pH=4的盐酸溶液等体积混合后,所得溶液的pH=。2.pH=2的盐酸和pH=5的硫酸溶液按体积比1:100混合后,所得溶液的pH=。1.pH=11的Ba(OH)2溶液与pH=9的NaOH溶液按体积比1∶1混合后的pH是________。2.pH=13的Ba(OH)2溶液与pH=10的NaOH溶液按体积比1∶1混合后的pH是

混合溶液的pH计算ppt课件.ppt
有关混合溶液pH的计算2.混合溶液的pH计算pH=9的NaOH溶液和pH=11的NaOH溶液等体积混合,求混合溶液的pH(3)强酸+强碱常温下,将0.3mol/L的盐酸和0.1mol/L的NaOH溶液各100mL混合,求混合溶液的pH常温下,将pH=2的硫酸900mL和pH=13的NaOH溶液100mL混合,求混合溶液的pH3.有关溶液的稀释pH=1的醋酸和盐酸均加水稀释,使体积为原来的1000倍则判断pH值正误(未给明条件时)不能用pH值等于多少来判断溶液酸、碱性。练习3室温时,下列溶液中碱性最强的是(

溶液的pH及计算-PPT课件.ppt
【例12】25℃,将pH=9与pH=12的两种强碱溶液等体积混合,求混合后溶液的pH结论⑷强碱与强碱混合【例14】25℃,将pH=2与pH=11的强酸和强碱溶液等体积混合,求混合后溶液的pH⑸强酸与强碱混合【例16】用纯水稀释pH=4的盐酸溶液至⑴10倍⑵100倍⑶1000倍⑷100000倍求稀释后溶液的pH。结论⑹稀释问题①若将强酸冲稀10n,pH增大n个单位,若弱酸稀释,每稀释10倍,pH增加小于1个单位但若无限冲稀,pH接近于7但小于7【例18】25℃,用纯水稀释pH=10的NaOH溶液至⑴10倍⑵

酸碱溶液pH的计算ppt课件.ppt
第三节酸碱溶液pH的计算物料平衡(MaterialBalanceEquilibrium,MBE):各物种的平衡浓度之和等于其分析浓度.电荷平衡(ChargeBalanceEquilibriua,CBE):溶液中正离子所带正电荷的总数等于负离子所带负电荷的总数.(电中性原则)质子条件(ProtonConditionEquilibriua,PCE):溶液中酸失去质子的数目等于碱得到质子的数目.例:HAc水溶液物料平衡式(MBE):c=[HAc]+[Ac-]电荷平衡式(CBE):[H+]=[Ac-]+[OH-]
