
化学能与电能PPT课件.ppt

ca****ng







亲,该文档总共20页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

化学能与电能ppt课件.pptx
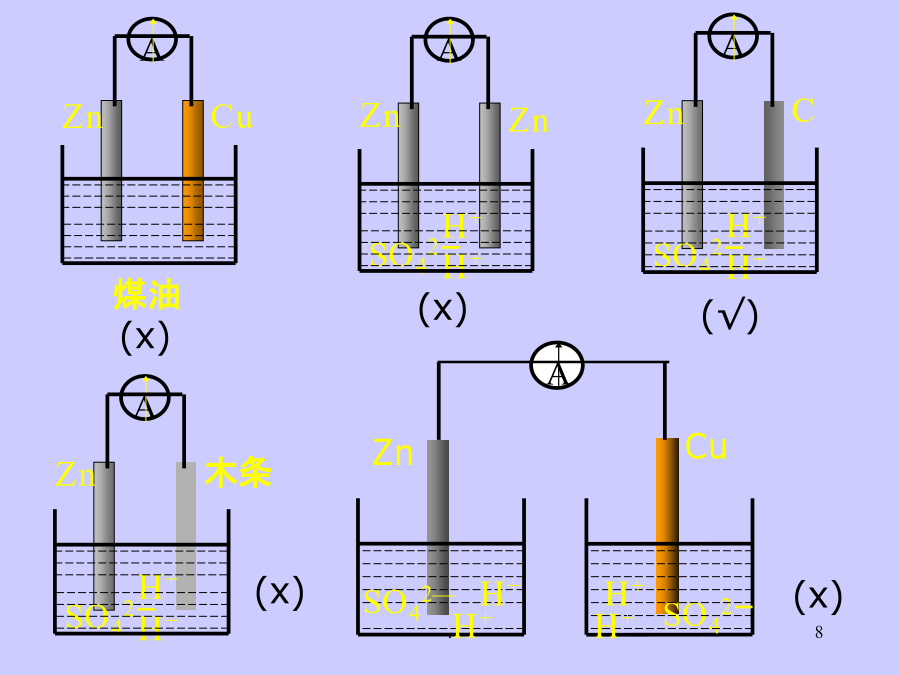
第二章化学反应与能量第二节《化学能与电能》第2课时1.掌握简单的电极反应的书写2.了解常见化学电池的组成与应用。3.了解新型燃料电池的组成和工作原理。判断下列几个学生设计的装置,能形成原电池的是?如果要设计一个原电池,思路如何?2.一个原电池的总反应的离子方程式Zn+Cu2+=Zn2++Cu,该反应的原电池的组成正确的是()6、设计原电池⑤实践活动:水果电池11二、发展中的化学电源化学电池干电池思考与交流:锌锰干电池即使不用,放置过久,也会失效(作为电解质的糊状NH4Cl显酸性),为了充分而有效地利用锌锰

化学能与电能ppt课件.ppt
第二节化学能与电能第二课时发展中的化学电源干电池(锌锰电池)使用最早的化学电池,属于一次性电池。二、发展中的化学电源(1)铅蓄电池最早使用的充电电池(1)铅蓄电池(2)镍镉充电电池:它是一种体积少,具有残留性记忆的充电电池,可重复使用500次以上。它以Cd为负极,NiO(OH)为正极,KOH为电解液。广泛用于收录机、无线对讲机、电子闪光灯、电动剃须刀等,但有毒,废旧电池要回收处理,防止污染环境。例1:蓄电池在放电时起原电池的作用,在充电时起电解池的作用。下面是爱迪生蓄电池分别在充电和放电时发生的反应:下列

化学能与电能PPT课件.ppt
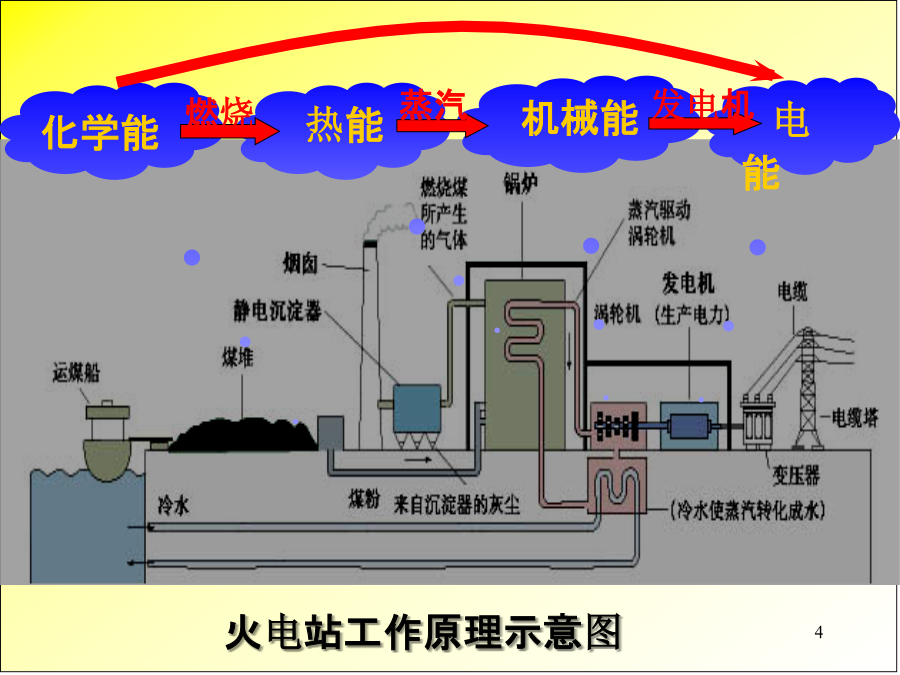
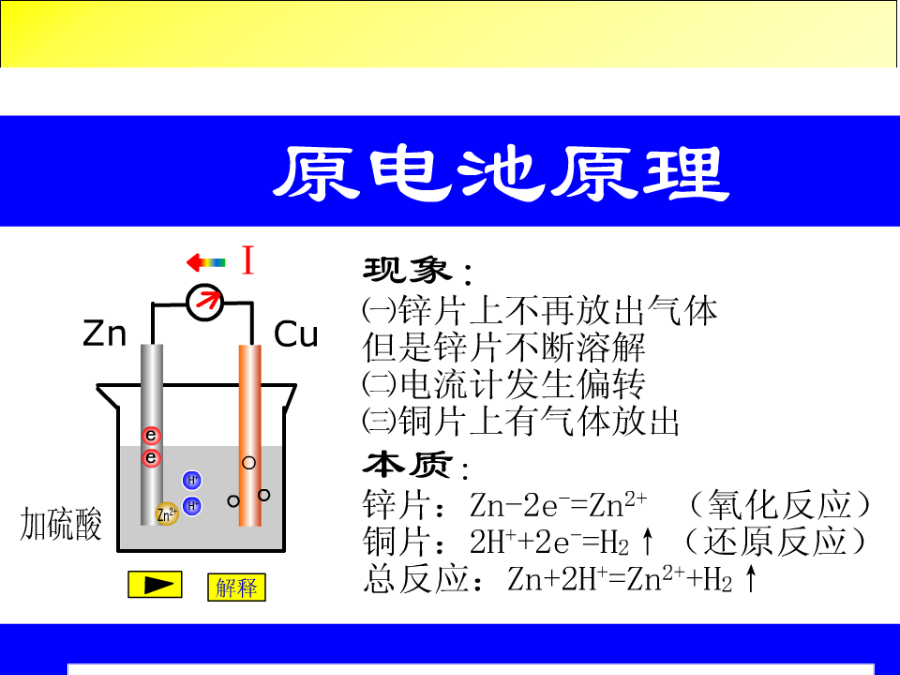
第二章化学反应与能量蒸汽2001年我国发电总量构成图火电站工作原理示意图54.构成原电池的条件一、化学能与电能的相互转化———原电池1、概念:将化学能转变为电能的装置2、反应本质:氧化还原反应3、原理:负极(锌片):Zn-2e-=Zn2+(氧化反应)正极(铜片):2H++2e-=H2↑(还原反应)总反应式:Zn+2H+=Zn2++H2↑4、原电池构成条件:5、原电池应用:(1)、判断金属的活泼性(2)、防止金属腐蚀(3)、提高化学反应速率(形成原电池反应,反应速率加快)Zn水果电池二、发展中的化学电源:1

化学能与电能PPT课件.ppt
第二节化学能与电能电能(电力):二次能源化学能热能机械能电能火力发电优点:1、初步了解原电池的概念、原理、组成及应用。2、通过实验探究从电子转移角度理解化学能向电能转化的本质及原电池的构成条件。【实验一】分别把锌片和铜片插入到稀H2SO4中,观察现象。【实验二】再用导线把锌片和铜片连接起来,观察铜片上有无气泡产生?一、原电池1、定义:把化学能转变为电能的装置.原电池电极材料实验探究:电极材料C4、原电池的构成条件6、原电池设计思路:请同学们根据原电池的原理,指出下列原电池的正极与负极分别是什么?写出电极反

化学能与电能ppt课件.pptx
第二章化学反应与能量第二节《化学能与电能》第2课时1.掌握简单的电极反应的书写2.了解常见化学电池的组成与应用。3.了解新型燃料电池的组成和工作原理。判断下列几个学生设计的装置,能形成原电池的是?如果要设计一个原电池,思路如何?2.一个原电池的总反应的离子方程式Zn+Cu2+=Zn2++Cu,该反应的原电池的组成正确的是()6、设计原电池⑤实践活动:水果电池11二、发展中的化学电源化学电池干电池思考与交流:锌锰干电池即使不用,放置过久,也会失效(作为电解质的糊状NH4Cl显酸性),为了充分而有效地利用锌锰
