
金属的电化学腐蚀和防护省公共课一等奖全国赛课获奖课件.pptx

ca****ng







亲,该文档总共23页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

金属的电化学腐蚀和防护省公共课一等奖全国赛课获奖课件.pptx
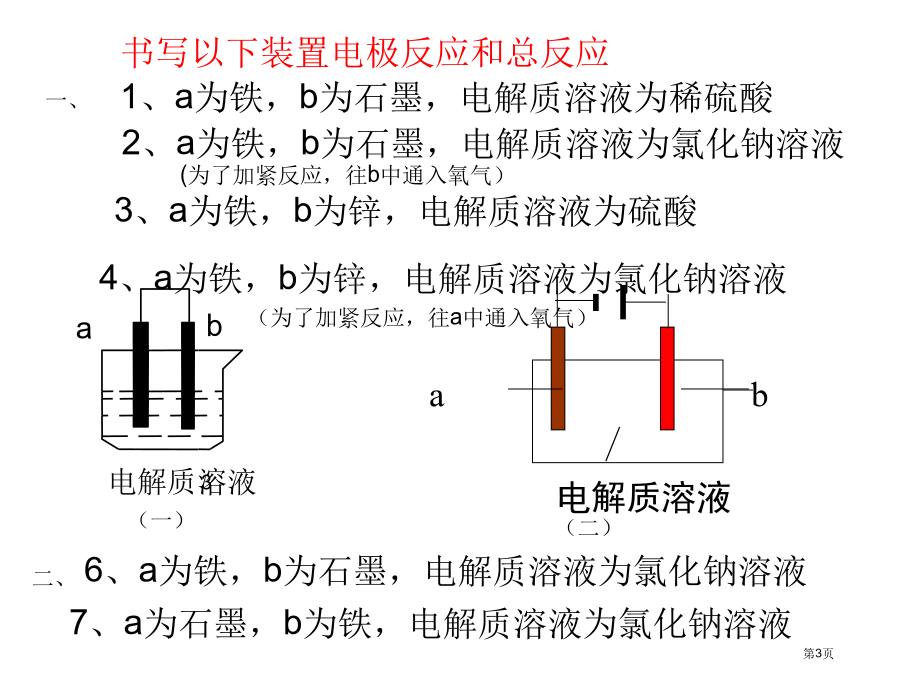
第四节金属电化学腐蚀与防护钢铁生锈书写以下装置电极反应和总反应我国作为世界上钢铁产量最多国家,每年被腐蚀铁占到我国钢铁年产量十分之一,因为金属腐蚀而造成损失占到国内生产总值2%~4%。金属腐蚀主要坏处,不但在于金属本身损失,更严重是金属制品结构损坏所造成损失比金属本身要大到无法估量。腐蚀不但造成经济损失,也经常对安全组成威胁。金属腐蚀钢铁在干燥空气里长时间不易被腐蚀,但在潮湿空气里却很快被腐蚀,这是什么原因呢?/10/10钢铁吸氧腐蚀示意图将用酸洗除锈铁钉,在饱和食盐水浸泡后放在如图所表示装置中,几分钟后

金属的电化学腐蚀和防护省公共课一等奖全国赛课获奖课件.pptx
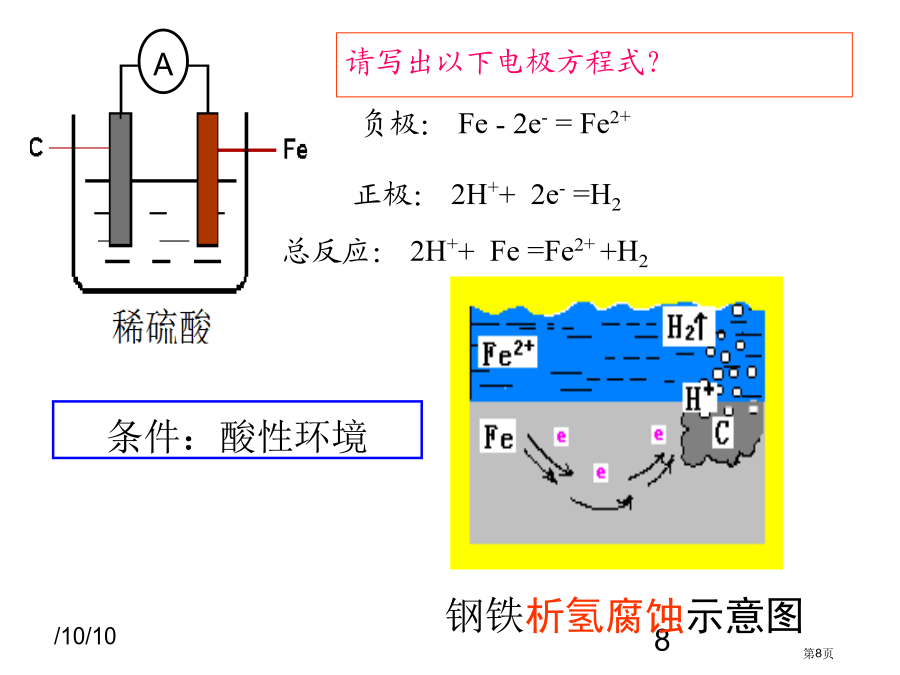
第四章电化学基础锈蚀轮船金属被腐蚀危害?全球每一分钟就有1吨钢腐蚀成铁锈.全世界每年因为金属腐蚀造成直接经济损失约达7000亿美元,是地震、水灾、台风等自然灾害造成损失总和6倍。全球每年钢铁腐蚀经济损失约占各国国民生产总值2%~4%,我国钢铁腐蚀经济损失高达2800亿人民币,约占国民生产总值4%,每年约有当年产量25%-30%钢铁因腐蚀而报废。腐蚀给人类造成损失是惊人。不纯金属跟电解质溶液接触时,会发生原电池反应,比较活泼金属失电子而被氧化腐蚀叫做电化学腐蚀。4、钢铁生锈原理钢铁吸氧腐蚀示意图钢铁析氢腐蚀

金属的电化学腐蚀及防护省公共课一等奖全国赛课获奖课件.pptx
【小测】写出以下溶液电解总反应式第4节:金属电化学腐蚀与防护钢铁生锈铜器生锈全球每一分钟就有1吨钢腐蚀成铁锈.全球每年钢铁腐蚀经济损失约10000亿美元,占各国国民生产总值GNP2%~4%.在美国,每年因钢铁腐蚀造成损失就占国内生产总值3%,大约三分之一化学设备因局部腐蚀而停工。我国钢铁腐蚀经济损失高达2800亿人民币,约占国民生产总值GNP4%,每年约有30%钢铁因腐蚀而报废。【阅读书本】P84-85回答以下问题:不纯金属(或合金)接触电解质溶液发生原电池反应,较活泼金属失去电子而被氧化所引发腐蚀。钢铁

金属电化学腐蚀与防护省公共课一等奖全国赛课获奖课件.pptx
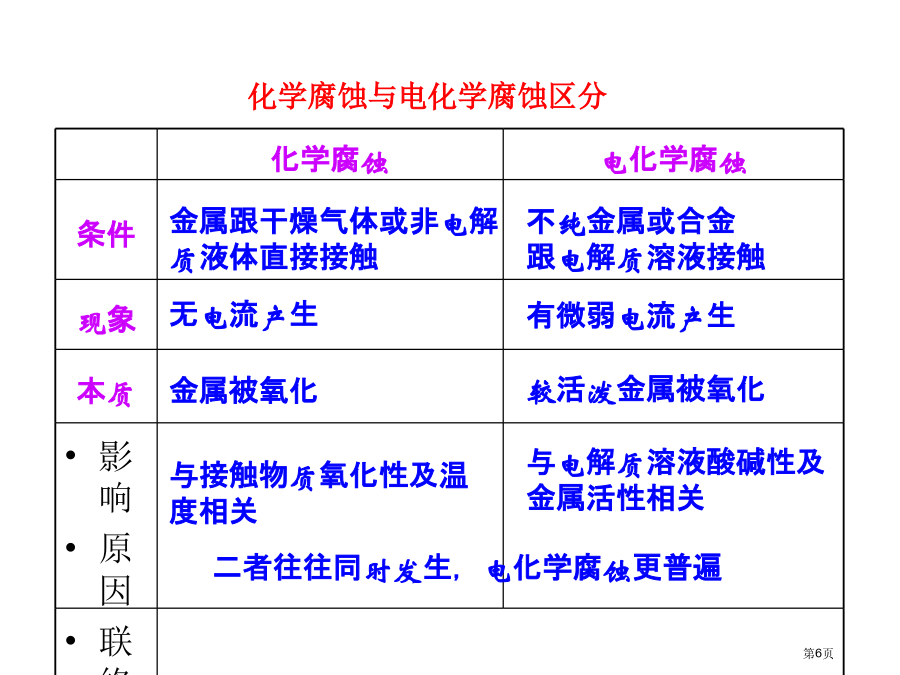
第四章电化学基础请比较以下Fe腐蚀快慢?金属腐蚀现象非常普遍:金属腐蚀现象非常普遍:8月1日,美国明尼苏达州一座跨越密西西比河大桥发生坍塌。事故造成6人死亡。金属制品腐蚀一、金属腐蚀本质:是金属或合金与周围接触到气体或液体发生氧化还原反应而引发损耗过程。M-ne-=Mn+二、金属腐蚀类型:(1)化学腐蚀金属跟接触到物质直接发生化学反应而引发腐蚀叫做化学腐蚀。(2)电化学腐蚀不纯金属跟电解质溶液接触时,会发生原电池反应,比较活泼金属失电子而被氧化腐蚀叫做电化学腐蚀。化学腐蚀和电化学腐蚀比较钢铁表面形成微小原

材料腐蚀和防护金属的电化学腐蚀省公共课一等奖全国赛课获奖课件.pptx
主要内容电化学腐蚀腐蚀原电池电极与电极电位标准电极定位及电动序---奈恩斯特(Nernst)方程式电极电位测定电化学反应热力学条件电位-PH图金属腐蚀本质:(按相互作用性质)腐蚀类型分为:化学腐蚀:金属与非电解质发生化学反应,氧化和还原在同一反应点瞬间同时完成;电化学腐蚀:金属与电解质发生电化学反应,氧化和还原相对独立且在金属表面不一样区域进行;第二节腐蚀原电池2.1腐蚀原电池模型物理学中要求,电流方向:电位高(正极)→电位低(负极)(即图中是电流方向是从cu片流向Zn片);电子流动方向则相反:电位低(负
