
(课标I)高考化学一轮复习 专题十一 化学能与热能课件-人教版高三全册化学课件精编.pptx

xf****65









亲,该文档总共72页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

(课标I)高考化学一轮复习 专题十一 化学能与热能课件-人教版高三全册化学课件精编.pptx
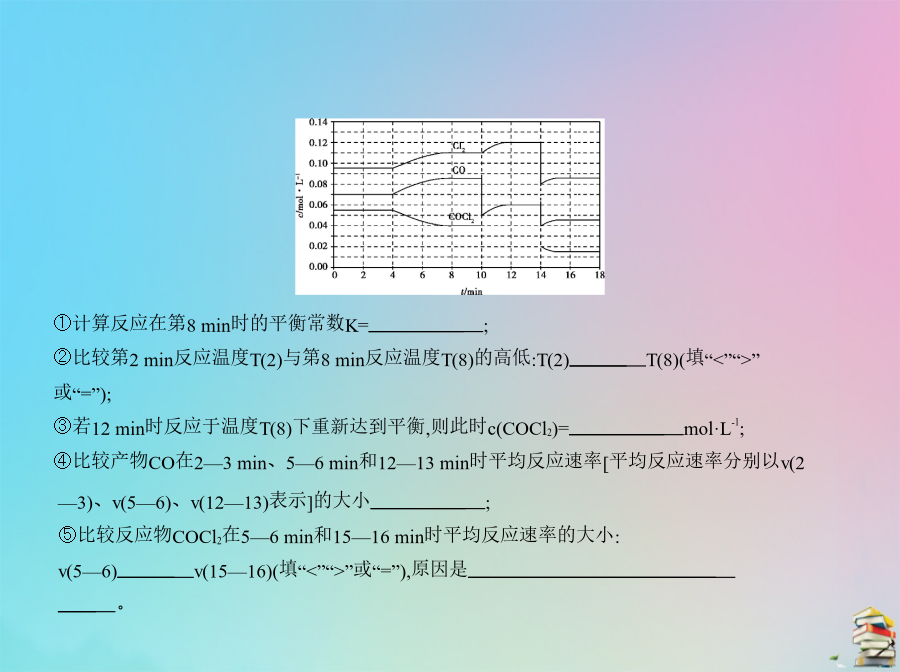
专题十一化学能与热能A组课标Ⅰ卷题组①计算反应在第8min时的平衡常数K=;②比较第2min反应温度T(2)与第8min反应温度T(8)的高低:T(2)T(8)(填“<”“>”或“=”);③若12min时反应于温度T(8)下重新达到平衡,则此时c(COCl2)=mol·L-1;④比较产物CO在2—3min、5—6min和12—13min时平均反应速率[平均反应速率分别以v(2答案(15分)(1)MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O(2)5.52×103kJ(3)CHCl3+H2O2 H

(课标I)高考化学一轮复习 专题十一 化学能与热能课件-人教版高三全册化学课件.pptx
专题十一化学能与热能A组课标Ⅰ卷题组①计算反应在第8min时的平衡常数K=;②比较第2min反应温度T(2)与第8min反应温度T(8)的高低:T(2)T(8)(填“<”“>”或“=”);③若12min时反应于温度T(8)下重新达到平衡则此时c(COCl2)=mol·L-1;④比较产物CO在2—3min、5—6min和12—13min时平均反应速率[平均反应速率分别以v(2答案(15分)(1)MnO2+4HCl(浓) MnCl2+Cl

(课标Ⅱ)高考化学一轮复习 专题十一 化学能与热能课件-人教版高三全册化学课件.pptx
专题十一化学能与热能考点一化学反应中能量变化的有关概念及计算由此计算ΔH1=kJ·mol-1;已知ΔH2=-58kJ·mol-1则ΔH3=kJ·mol-1。(2)反应①的化学平衡常数K表达式为;图1中能正确反映平衡常数K随温度变化关系的曲线为(填曲线标记字母)其判断理由是。 图1

(课标版)高考化学一轮复习 专题十一 化学能与热能课件-人教版高三全册化学课件.pptx
考点一反应热的有关概念6.产生原因:化学反应过程中旧键断裂吸收的能量与新键形成放出的能量不相等故化学反应均伴随着能量变化。二、燃烧热和中和反应的反应热1.燃烧热2.中和反应的反应热(1)定义:在稀溶液中酸跟碱发生⑨中和反应生成 1molH2O时所释放的热量叫作中和反应的反应热。(2)热化学方程式:H+(aq)+OH-(aq) H2O(l)ΔH=-57.3kJ·mol-1。三、催化剂对活化能、焓变的影响重点突破一、放热反应和吸热反应的比较二、常见的放热反应和吸热反应1.常见的放热反

(新课标Ⅰ)高考化学一轮复习 专题五 化学能与热能课件-人教版高三全册化学课件精编.ppt
专题五化学能与热能考点一化学反应中能量变化的有关概念及计算1.(2015课标Ⅱ,27,14分,0.321)甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:①CO(g)+2H2(g) CH3OH(g)ΔH1②CO2(g)+3H2(g) CH3OH(g)+H2O(g)ΔH2③CO2(g)+H2(g) CO(g)+H2O(g)ΔH3回答下列问题:(1)已知反应①中相关的化学键键能数据如下:由此计算ΔH1=kJ·mol-1;已知ΔH2=-
