
试题-浙江-2014_浙江省宁波市效实中学2015届高三化学上学期期中试题(含解析).rar

曾琪****是我










亲,该文档总共23页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

试题-浙江-2014_浙江省宁波市效实中学2015届高三化学上学期期中试题(含解析).rar
-23-化学试卷一、选择题(每小题2分,共20分.每小题只有一个选项符合题意.)1.(2分)化学在生产和日常生活中有着重要的应用.下列说法正确是()A.高纯度的硅单质广泛用于制作光导纤维B.向煤中加入适量石灰石,在煤燃烧时SO2最终生成CaSO3,可减少对大气的污染C.汽车的排气管上装有“催化转化器”,使有毒的CO和NO反应生成N2和CO2D.大量燃烧化石燃料排放的废气中含大量CO2、SO2造成大气污染,从而使雨水pH=5.6形成酸雨考点:硅和二氧化硅;二氧化硫的污染及治理;常见的生活环境的污染及治理..
试题-浙江-2014_浙江省效实中学2015届高三化学上学期期中试题.rar
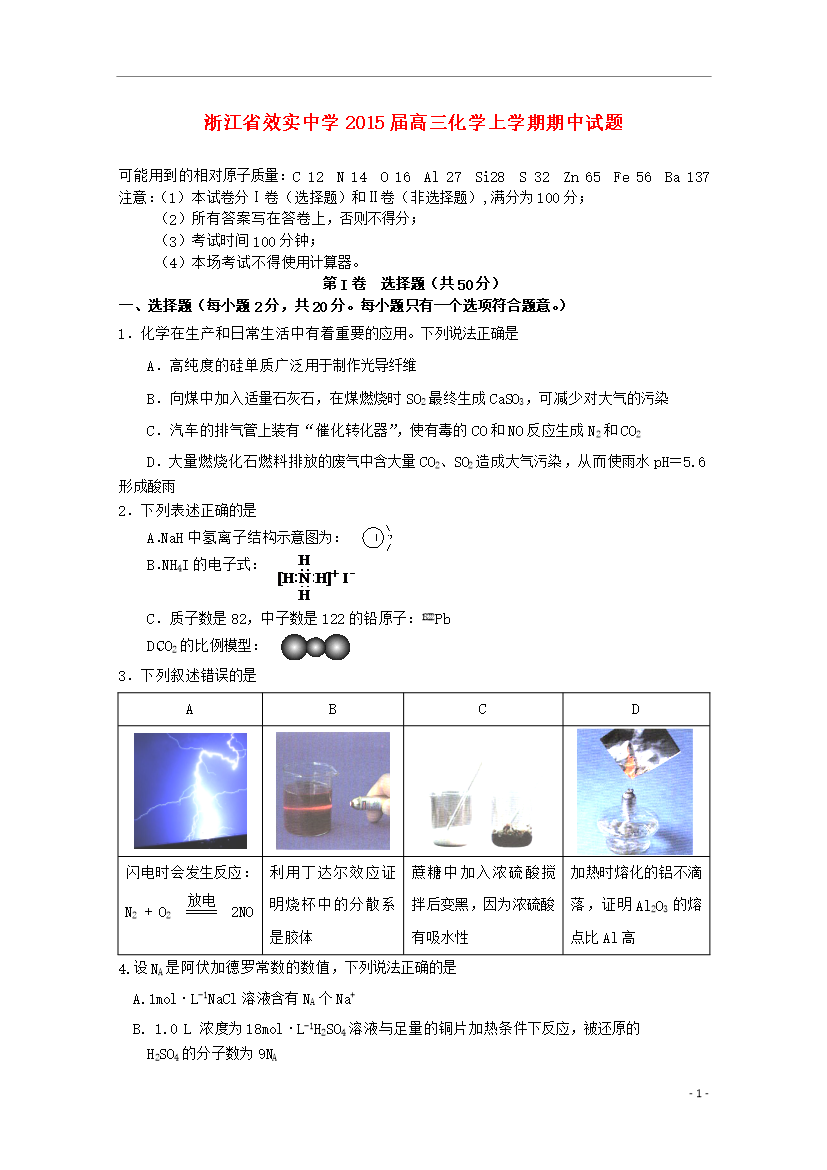
-9-浙江省效实中学2015届高三化学上学期期中试题可能用到的相对原子质量:C12N14O16Al27Si28S32Zn65Fe56Ba137注意:(1)本试卷分Ⅰ卷(选择题)和Ⅱ卷(非选择题),满分为100分;(2)所有答案写在答卷上,否则不得分;(3)考试时间100分钟;(4)本场考试不得使用计算器。第I卷选择题(共50分)一、选择题(每小题2分,共20分。每小题只有一个选项符合题意。)1.化学在生产和日常生活中有着重要的应用。下列说法正确是A.高纯度的硅单质广泛用于制作光导纤维B.向煤中加入适量石灰

浙江省宁波市效实中学2016届高三语文上学期期中试题含解析.doc
-14-效实中学2015学年第一学期高三期中试卷语文试题卷一、语言文字运用(共24分其中选择题每小题3分)1.下列词语中加点字的注音有误的一项是()A.畚(běn)箕椪(pèng)柑堰(yàn)塞湖扺(zhǐ)掌而谈B.孢(bāo)子蛤(gé)蜊应(yīng)届生便(biàn)宜从事C.秕(bǐ)谷蹁(pián)跹发横(hèng)财人影幢幢(chuáng)D.鳊(biān)鱼亲(qìn)家青

浙江省宁波市效实中学2021届高三英语上学期期中试题(含解析).doc
浙江省宁波市效实中学2021届高三英语上学期期中试题(含解析)1.本试题卷满分150分,考试时间120分钟。2.答题前,请务必在答题卷指定区域填写班级、姓名、考场号、座位号及准考证号并填涂相应数字;3.答题时,请按照答题纸上“注意事项”的要求,在答题纸相应的位置上规范作答,在本试题卷上的作答一律无效;4.非选择题的答案必须使用黑色字迹的签字笔或钢笔写在答题纸上相应区域内。选择题部分第一部分听力(共两节,满分30分)做题时,先将答案标在试卷上。录音内容结束后,你将有两分钟的时间将试卷上的答案转涂到答题纸上。

浙江省宁波市效实中学2021届高三英语上学期期中试题(含解析).doc
24浙江省宁波市效实中学2021届高三英语上学期期中试题(含解析)1.本试题卷满分150分,考试时间120分钟。2.答题前,请务必在答题卷指定区域填写班级、姓名、考场号、座位号及准考证号并填涂相应数字;3.答题时,请按照答题纸上“注意事项”的要求,在答题纸相应的位置上规范作答,在本试题卷上的作答一律无效;4.非选择题的答案必须使用黑色字迹的签字笔或钢笔写在答题纸上相应区域内。选择题部分第一部分听力(共两节,满分30分)做题时,先将答案标在试卷上。录音内容结束后,你将有两分钟的时间将试卷上的答案转涂到答题纸
