
医学胶体医学知识宣讲PPT培训课件.pptx

13****54








亲,该文档总共59页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

医学胶体医学知识宣讲PPT培训课件.pptx
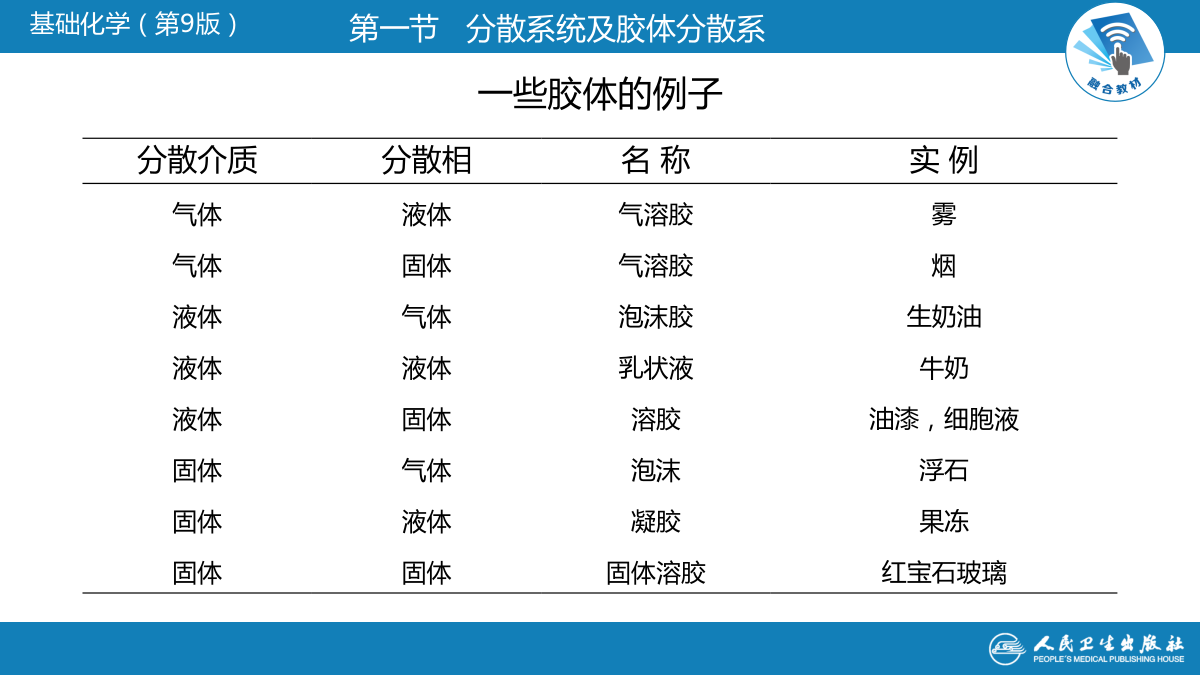
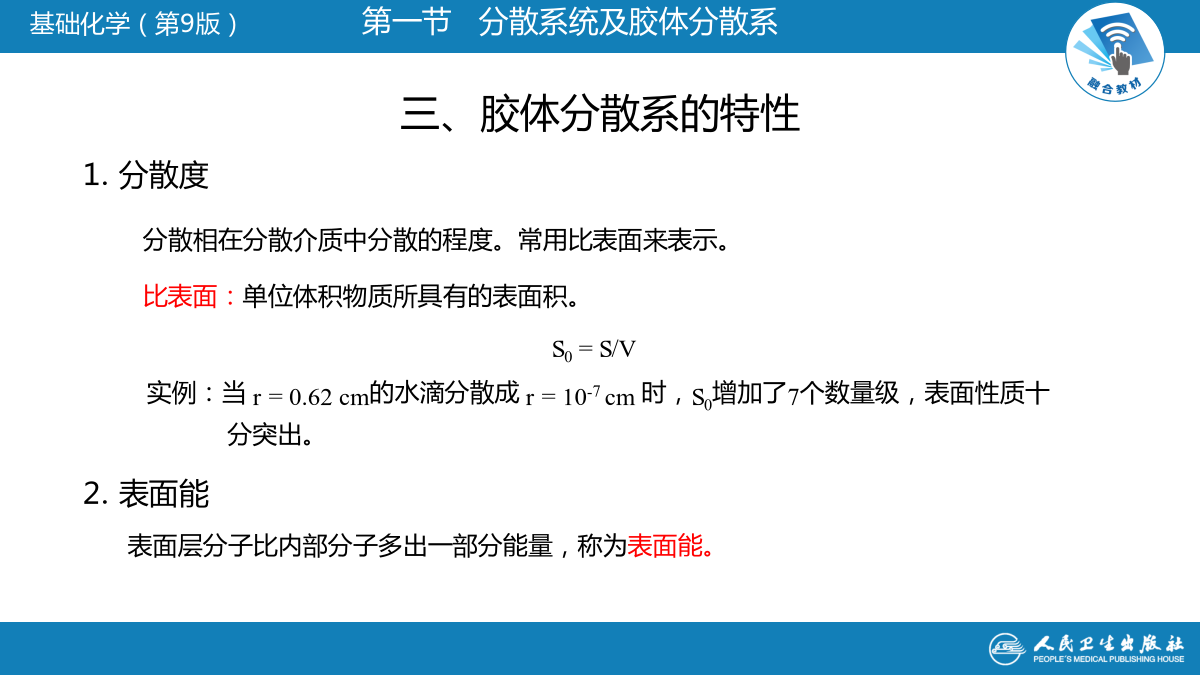
胶体医学知识宣讲溶胶的基本性质;胶团结构及表示式;溶胶的稳定性因素及聚沉作用。分散系统及胶体分散系一、分散系统及其分类分散系的分类二、胶体分散系一些胶体的例子三、胶体分散系的特性液体、固体有自动缩小表面积的趋势。小液滴聚集变大缩小表面积,可降低表面能。表面积减小过程是自发过程。这个结论对固体物质同样适用。高度分散的溶胶比表面大,所以表面能也大,它们有自动聚积成大颗粒而减少表面积的趋势,称为聚结不稳定性。界面:相与相之间的接触面如:液-气、固-气、液-液、固-液等表面:液-气界面、固-气界面溶胶分散相:胶粒

医学糖类医学知识宣讲PPT培训课件.pptx
糖类医学知识宣讲重点难点单糖有机化学(第9版)有机化学(第9版)有机化学(第9版)有机化学(第9版)有机化学(第9版)有机化学(第9版)有机化学(第9版)有机化学(第9版)有机化学(第9版)有机化学(第9版)有机化学(第9版)有机化学(第9版)有机化学(第9版)有机化学(第9版)有机化学(第9版)有机化学(第9版)有机化学(第9版)有机化学(第9版)有机化学(第9版)有机化学(第9版)有机化学(第9版)有机化学(第9版)双糖和多糖有机化学(第9版)有机化学(第9版)有机化学(第9版)有机化学(第9版)有机

医学肺癌医学知识宣讲PPT培训课件.pptx
肺癌医学知识宣讲重点难点原发性支气管癌:起源于呼吸上皮细胞(支气管、细支气管和肺泡)的恶性肿瘤最常见的肺部原发性恶性肿瘤发病高峰在55~65岁,男性多于女性以咳嗽、咳痰、咯血和消瘦等为主要表现影像学:肺部结节、肿块影多数病人确诊时已是晚期,5年生存率低于20%肺癌是全球癌症相关死亡最主要的原因WHO2012年:全球新发肺癌182.5万,占所有癌症13.0%肺癌死亡数159.0万,占所有癌症死亡19.4%中国2015年:新发肺癌73.3万,肺癌死亡61.0万男性发病率列所有癌症首位,女性仅次于乳腺癌,死亡率

医学胸腔医学知识宣讲PPT培训课件.ppt
胸腔医学知识宣讲一、胸膜及胸膜腔(二)胸膜腔胸膜隐窝:肋膈隐窝肋纵隔隐窝施行胸膜腔穿刺术需经过哪些层次?临床行胸膜腔穿刺术(抽液)常选在肩胛线或腋后线、第7或8肋间隙中部或肋上缘稍上方进针。分部胸骨部:起自剑突后面肋部:起自下6对肋骨和肋软骨的内面腰部:以左、右膈脚起自上2-3个腰椎止点:中心腱膈的三个裂孔腔静脉孔:平T8胸椎,通过下腔静脉、右膈神经的分支食管裂孔:平T10胸椎,食管、迷走神经、胃左血管的食管支和淋巴管通过。裂孔与食管间有韧带,孔周围有肌环,可固定食管。主动脉裂孔:平第12胸椎,胸导管、主

医学胃癌医学知识宣讲PPT培训课件.pptx
胃癌医学知识宣讲重点难点隆起内科学(第9版)三、胃癌的诊断内科学(第9版)内科学(第9版)
