
现代分析测试技术-热分析技术ppt课件.ppt

天马****23








亲,该文档总共56页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

现代分析测试技术-热分析技术ppt课件.ppt
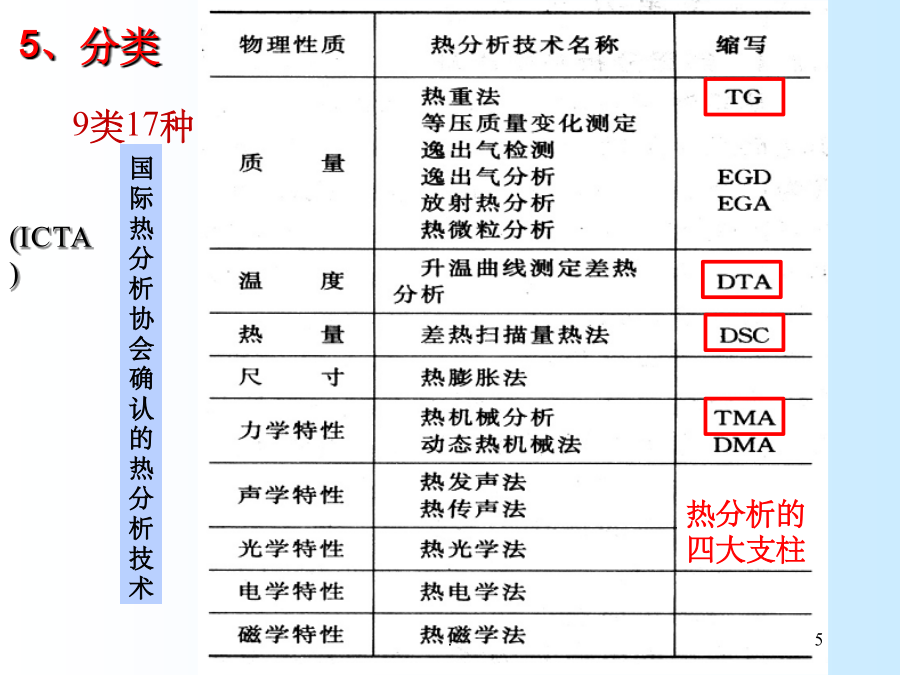
补充内容二热分析技术ThermalAnalysis1887年,法(德)国人第一次用热电偶测温的方法研究粘土矿物在升温过程中的热性质的变化。1891年,英国人使用示差热电偶和参比物,记录样品与参照物间存在的温度差,大大提高了测定灵敏度,发明了差热分析(DTA)技术的原始模型。1915年,日本人在分析天平的基础上研制出热天平,开创了热重分析(TG)技术。1940-1960年,热分析向自动化、定量化、微型化方向发展。1964年,美国人在DTA技术的基础上发明了示差扫描量热法(DSC),Perkin-Elmer公

现代分析测试技术热分析技术专题培训课件.ppt
现代分析测试技术热分析技术PPT讲座1887年,法(德)国人第一次用热电偶测温的方法研究粘土矿物在升温过程中的热性质的变化。1891年,英国人使用示差热电偶和参比物,记录样品与参照物间存在的温度差,大大提高了测定灵敏度,发明了差热分析(DTA)技术的原始模型。1915年,日本人在分析天平的基础上研制出热天平,开创了热重分析(TG)技术。1940-1960年,热分析向自动化、定量化、微型化方向发展。1964年,美国人在DTA技术的基础上发明了示差扫描量热法(DSC),Perkin-Elmer公司率先研制了D

现代分析测试技术-热分析技术.ppt
补充内容二热分析技术ThermalAnalysis1887年,法(德)国人第一次用热电偶测温的方法研究粘土矿物在升温过程中的热性质的变化。1891年,英国人使用示差热电偶和参比物,记录样品与参照物间存在的温度差,大大提高了测定灵敏度,发明了差热分析(DTA)技术的原始模型。1915年,日本人在分析天平的基础上研制出热天平,开创了热重分析(TG)技术。1940-1960年,热分析向自动化、定量化、微型化方向发展。1964年,美国人在DTA技术的基础上发明了示差扫描量热法(DSC),Perkin-Elmer公

现代分析测试技术-热分析技术.ppt
12345678910111213141516171819202122232425262728293031323334353637383940414243DSC-2C型示差扫描量热计3、典型的DSC曲线4、DSC与DTA的区别DSC5、示差扫描量热分析法的影响因素(一)实验条件的影响⑴升温速率程序升温速率主要影响DSC曲线的峰温和峰形。⑵气体性质(二)试样特性的影响⑴试样用量⑵试样粒度⑶试样的几何形状4950515253545556

现代分析测试技术-热分析技术.ppt
12345678910111213141516171819202122232425262728293031323334353637383940414243DSC-2C型示差扫描量热计3、典型的DSC曲线4、DSC与DTA的区别DSC5、示差扫描量热分析法的影响因素(一)实验条件的影响⑴升温速率程序升温速率主要影响DSC曲线的峰温和峰形。⑵气体性质(二)试样特性的影响⑴试样用量⑵试样粒度⑶试样的几何形状4950515253545556
