
试题-全国-2008_2008年高考化学最后预测20题.rar

An****70









在线预览结束,喜欢就下载吧,查找使用更方便
相关资料

试题-全国-2008_2008年高考化学最后预测20题.rar
用心爱心专心115号编辑2008年高考化学最后预测20题1.下列变化不能说明发生了化学变化的是CA.变化时有电子的得失或共用电子对的形成B.变化过程中有化学键的断裂和形成C.变化时释放出能量D.变化前后原子的种类和数目没有改变,分子种类增加了2.关于元素周期表的说法不正确的是AA.元素周期表有8个主族B.ⅠA族的元素不全是金属元素C.元素周期表有7个周期D.短周期是指第一、二、三、四周期3.为提纯下列物质(括号内的物质是杂质),所选用的除杂试剂和分离方法都正确的是C被提纯的物质除杂试剂分离方法A溴化钠溶液
试题-全国-2008_2008年高考化学最后预测20题题.rar
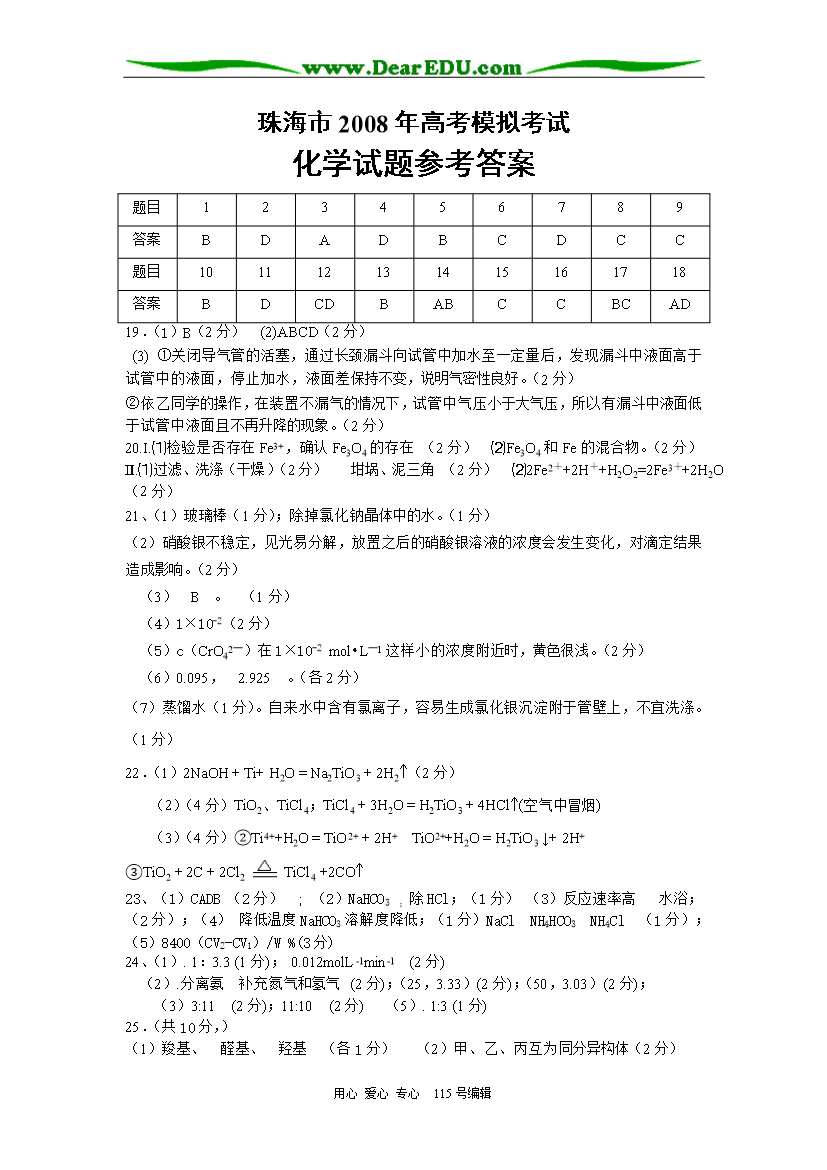
用心爱心专心115号编辑珠海市2008年高考模拟考试化学试题参考答案题目123456789答案BDADBCDCC题目101112131415161718答案BDCDBABCCBCAD19.(1)B(2分)(2)ABCD(2分)(3)①关闭导气管的活塞,通过长颈漏斗向试管中加水至一定量后,发现漏斗中液面高于试管中的液面,停止加水,液面差保持不变,说明气密性良好。(2分)②依乙同学的操作,在装置不漏气的情况下,试管中气压小于大气压,所以有漏斗中液面低于试管中液面且不再升降的现象。(2分)20.I.⑴检验是否存

试题-全国-2008_2008年高考化学预测.rar
用心爱心专心116号编辑2008年高考预测—化学(1)一、新增内容预测(一)新增考点:环境保护1.旨在遏制全球气候变暖的《京都议定书》2005年2月16日正式生效,受到限制的气体包括人为排出的二氧化碳、甲烷、一氧化氮、氟化烃、全氟化碳以及六氟化硫六种气体的排放量。下列有关说法正确的是A.控制温室气体排放,遏制全球变暧趋势是社会可持续发展的保证B.CH4是目前全球变暧的最主要的温室气体C.NO不仅能引起温室效应还与臭氧层破坏、酸雨及化学烟雾有关D.CO2、CF3Cl、C3F8、SF6分子中所有原子均满足八电

试题-全国-2008_2008年高考化学选择题预测.rar
用心爱心专心115号编辑2008年高考化学选择题预测一.单项选择题(每小题有仅有一个选项符合题意)1996年诺贝尔化学奖授于斯莫利等三位化学家,以表彰他们发现富勒烯(C60)开辟了化学研究的新领域。后来,人们又发现了一种含碳量极高的链式炔烃──棒碳,它是分子中含300~500个碳原子的新物质,其分子中只含有交替连接的单键和叁键。试根据上述信息回答1.2两小题:1.对于C60与棒碳,下列说法正确的是()A.C60在一定条件下可能与CuO发生置换反应B.棒碳不能使溴水褪色C.C60与棒碳中所有的化学键都是非极

试题-全国-2008_2008年广东高考化学预测卷.rar
用心爱心专心115号编辑2008年广东高考预测卷--化学可能用到的相对原子质量:H~1,C~12,N~14,O~16,Na~23,S~32,Cl~35.5,K~39,Ca~40,Fe~56,Cu~64,Zn~65。第I卷(选择题共63分)一、选择题(本大题包括9个小题,共27分。每小题只有一个选项符合题意)1、将氯化铁饱和溶液逐滴加入沸水中,制得氢氧化铁胶体溶液,为了除去其中所含的盐酸,得到较纯净的氢氧化铁胶体,应采取的措施是A、加入NaOH溶液进行中和B、加入AgNO3溶液反应后过滤C、插入石墨电极,通
