
试题-全国-2014_2014高考化学 突破课时训练 专题七 电解质溶液.rar

猫巷****松臣







在线预览结束,喜欢就下载吧,查找使用更方便
相关资料
试题-全国-2014_2014高考化学 突破课时训练 专题七 电解质溶液.rar
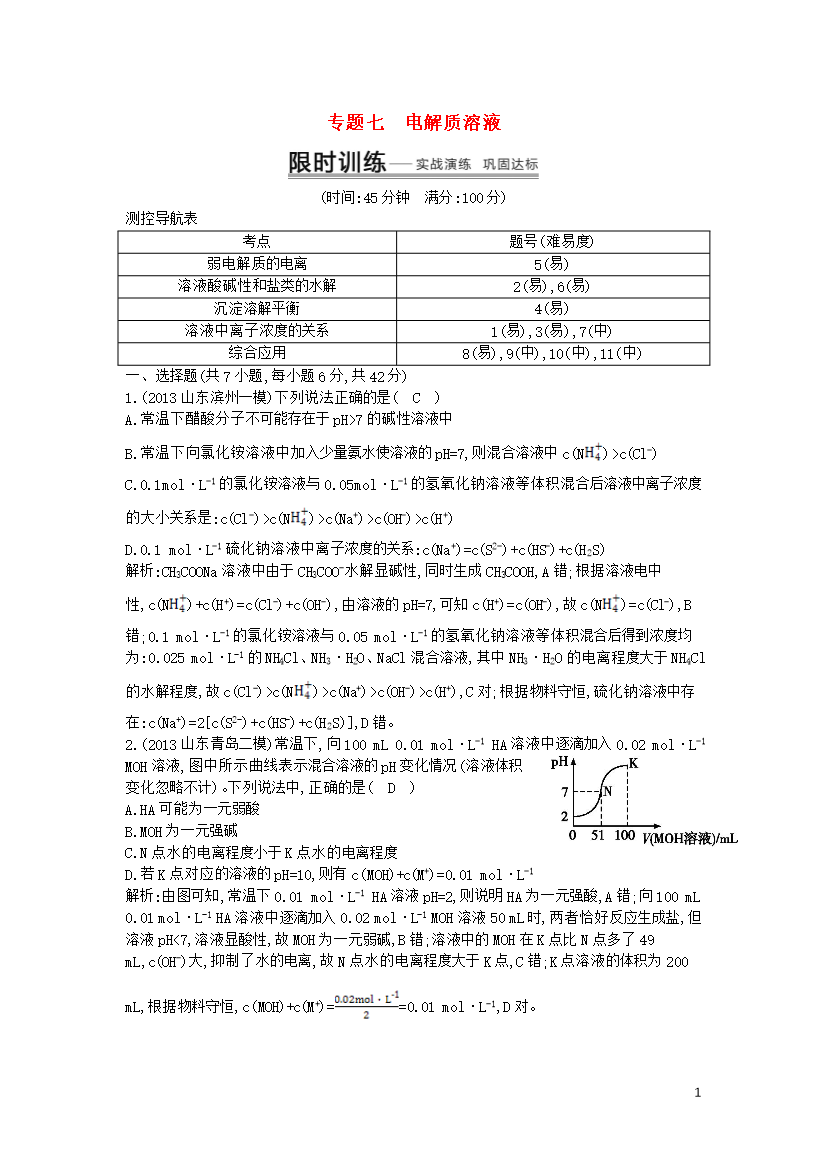
7专题七电解质溶液(时间:45分钟满分:100分)测控导航表考点题号(难易度)弱电解质的电离5(易)溶液酸碱性和盐类的水解2(易),6(易)沉淀溶解平衡4(易)溶液中离子浓度的关系1(易),3(易),7(中)综合应用8(易),9(中),10(中),11(中)一、选择题(共7小题,每小题6分,共42分)1.(2013山东滨州一模)下列说法正确的是(C)A.常温下醋酸分子不可能存在于pH>7的碱性溶液中B.常温下向氯化铵溶液中加入少量氨水使溶液的pH=7,则混合溶液中c(N)>c(Cl-)C.0.1mol·L

2014高考化学 突破课时训练 专题七 电解质溶液.doc
专题七电解质溶液(时间:45分钟满分:100分)测控导航表考点题号(难易度)弱电解质的电离5(易)溶液酸碱性和盐类的水解2(易),6(易)沉淀溶解平衡4(易)溶液中离子浓度的关系1(易),3(易),7(中)综合应用8(易),9(中),10(中),11(中)一、选择题(共7小题,每小题6分,共42分)1.(2013山东滨州一模)下列说法正确的是(C)A.常温下醋酸分子不可能存在于pH>7的碱性溶液中B.常温下向氯化铵溶液中加入少量氨水使溶液的pH=7,则混合溶液中c(N)>c(Cl-)C.0.1mol·L-

试题-全国-2014_2014高考化学 突破课时训练 专题二 化学常用计量 溶液.rar
5专题二化学常用计量溶液(时间:45分钟满分:100分)测控导航表考点题号(难易度)以物质的量为中心的相关计算5(易),10(中)阿伏加德罗常数及其应用1(易),2(易),3(易),4(易),6(易),9(易)物质的量浓度及溶液配制8(易),11(易)综合7(易),12(中)一、选择题(共10小题,1~5每小题6分,6~10每小题7分,共65分)1.(2013陕西西安模拟)下列说法正确的是(C)A.2.24LCO2中共有的原子数为0.3×6.02×1023B.1.8gN共有的质子数为6.02×1023C.

试题-全国-2014_2014高考化学二轮专题突破练 专题十电解质溶液.rar
262014高考化学二轮专题突破练:专题十电解质溶液[考纲要求]1.了解电解质在水溶液中的电离,以及电解质溶液的导电性;了解电解质的概念;了解强弱电解质的概念。2.了解弱电解质在水溶液中的电离平衡。3.了解水的电离,水的离子积常数。4.了解溶液pH的定义;了解测定溶液pH的方法,能进行pH的简单计算。5.了解盐类水解的原理、影响盐类水解程度的主要因素以及盐类水解的应用。6.了解难溶电解质的沉淀溶解平衡及沉淀转化的本质。7.以上各部分知识的综合利用。考点一溶液的酸碱性及pH计算1.一个基本不变相同温度下,不

高考化学复习专题训练:电解质溶液.doc
2019年高考化学复习专题训练:电解质溶液下面是编辑老师整理的2019年高考化学复习专题训练:电解质溶液希望对您提高学习效率有所帮助.1.(2019福建理综10)下列关于0.10molL-1NaHCO3溶液的说法正确的是()A.溶质的电离方程式为NaHCO3Na++H++COB.25℃时加水稀释后n(H+)与n(OH-)的乘积变大C.离子浓度关系:c(Na+)+c(H+)=c(OH-)+c(HCO)+c(CO)D.温度升高c(HCO)增大答案B解析A项H2CO3为弱电解质HCO在
