
微管及其功能PPT.ppt

天马****23









亲,该文档总共32页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

微管及其功能PPT.ppt
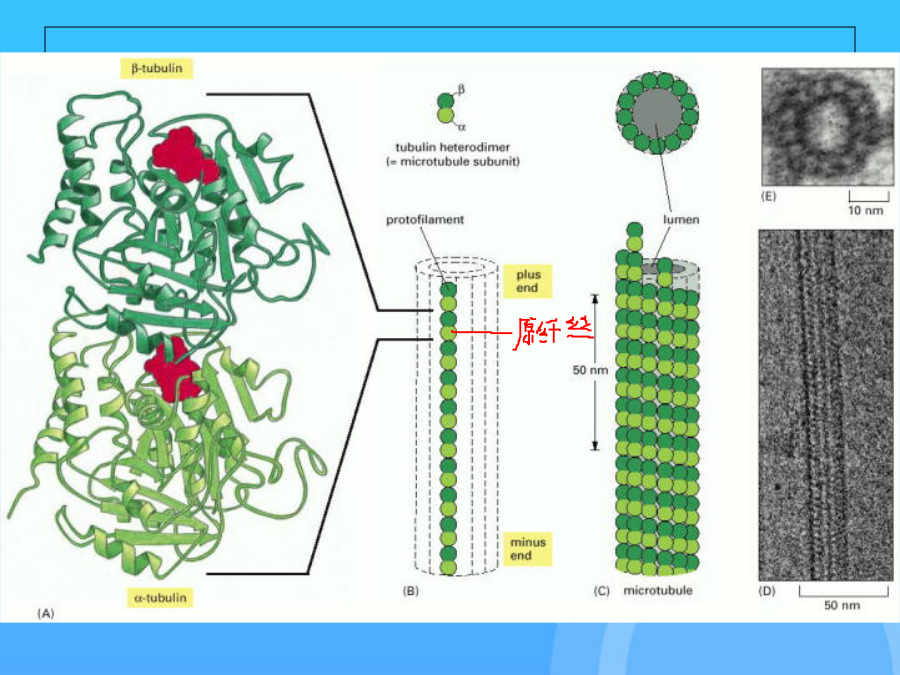
微管及其功能(优选)第二节微管及其功能一、微管的结构组成与极性13二、微管的组装和去组装微管在体外的组装过程可分为成核和延伸两个阶段。①一些微管蛋白(α微管蛋白和β微管蛋白)二聚体(①αβ二聚体)首先纵向聚合形成短的丝状结构(②原纤维),即所谓的成核反应②然后通过两端以及侧面增加二聚体而扩展成片状,当片状聚合物加宽到大致13根原纤丝时,即合拢成为一段微管(③微管)。新的微管蛋白二聚体不断地组装到这段微管的两端,使之延长作用于微管的特异性药物三、微管组织中心中心体基体和其他微管组织中心微管的动力学性质五、微

微管及其功能ppt课件.ppt
第二节微管及其功能一、微管的结构组成与极性13二、微管的组装和去组装微管在体外的组装过程可分为成核和延伸两个阶段。①一些微管蛋白(α微管蛋白和β微管蛋白)二聚体(①αβ二聚体)首先纵向聚合形成短的丝状结构(②原纤维),即所谓的成核反应②然后通过两端以及侧面增加二聚体而扩展成片状,当片状聚合物加宽到大致13根原纤丝时,即合拢成为一段微管(③微管)。新的微管蛋白二聚体不断地组装到这段微管的两端,使之延长作用于微管的特异性药物三、微管组织中心中心体基体和其他微管组织中心微管的动力学性质五、微管结合蛋白对微管网络

微管蛋白甲基化修饰对微管功能的影响及其机制.docx
微管蛋白甲基化修饰对微管功能的影响及其机制标题:微管蛋白甲基化修饰对微管功能的影响及其机制摘要:微管是细胞骨架的重要组成部分,参与细胞的形态维持、细胞极性和细胞分裂等关键生理过程。微管蛋白甲基化修饰是最近研究中的一个热点话题,已经证实与微管的结构稳定性、动态极性调节以及微管相关细胞过程密切相关。本文将综述微管蛋白甲基化修饰对微管功能的影响以及其机制的研究进展,旨在加深对这一领域的深入理解。关键词:微管;蛋白甲基化;修饰;功能;机制1.引言微管是由αβ二聚体组成的管状结构,具有生长和萎缩的动态性,并参与细胞

α--微管蛋白的SUMO1化修饰及其对微管功能的影响.docx
α--微管蛋白的SUMO1化修饰及其对微管功能的影响α-微管蛋白的SUMO1化修饰及其对微管功能的影响摘要:微管是细胞内重要的细胞骨架成分,参与了细胞的结构和运动调节。近年来的研究表明,微管蛋白的修饰对微管的功能具有重要影响。SUMO1是一种小的蛋白质后修饰,被广泛修饰目标蛋白。本文综述了SUMO1化修饰对α-微管蛋白的影响,特别是对微管功能的调节机制,并指出了未来相关研究的发展方向。引言:微管是由α-微管蛋白组成的网络结构,参与了细胞的极性、分裂、运输等重要过程。微管蛋白主要分为α、β、γ三个亚单位,其
第2节:微管及其功能.pdf
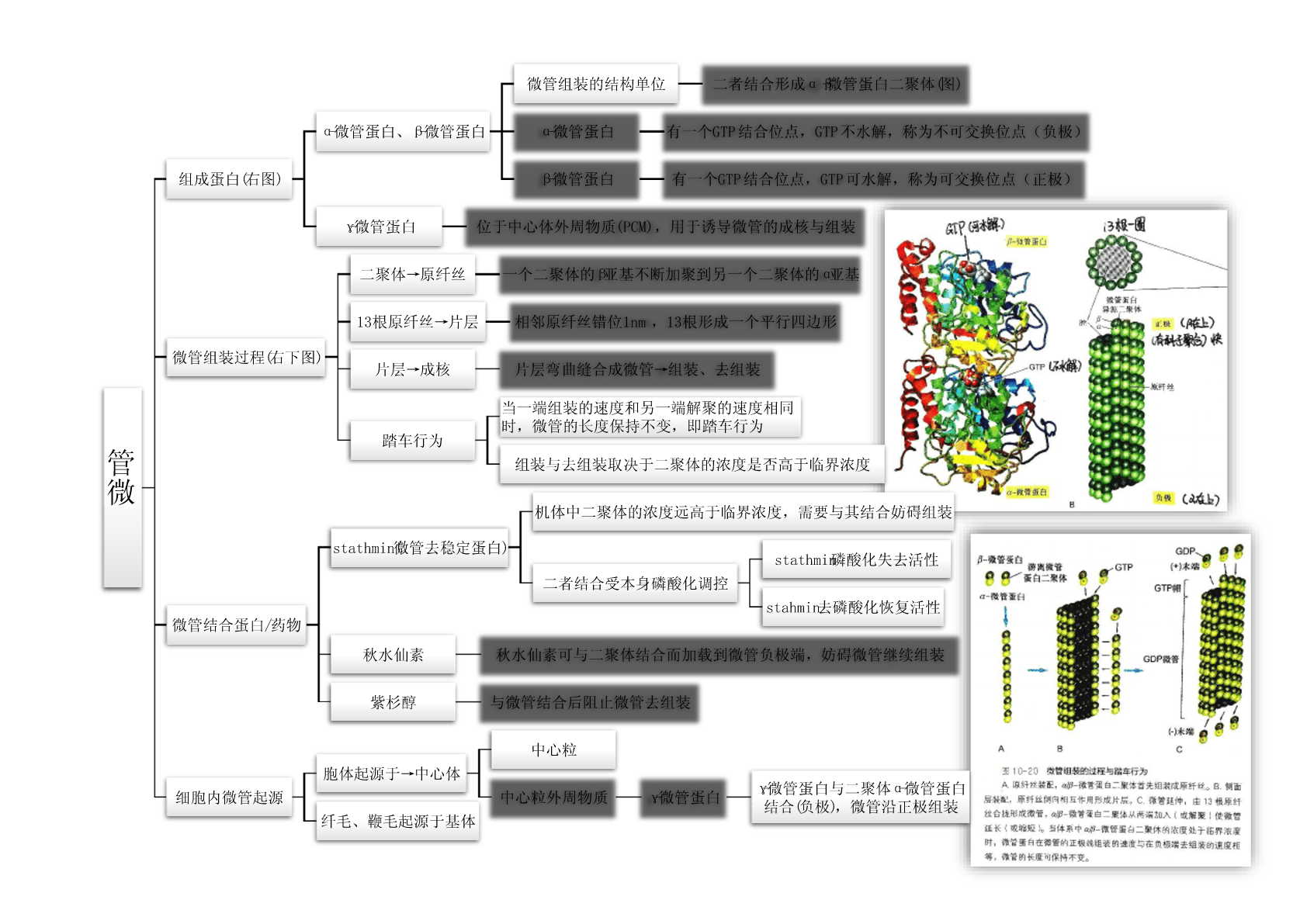
微管组装的结构单位二者结合形成αβ-微管蛋白二聚体(图)α-微管蛋白、β-微管蛋白α-微管蛋白有一个GTP结合位点,GTP不水解,称为不可交换位点(负极)组成蛋白(右图)β-微管蛋白有一个GTP结合位点,GTP可水解,称为可交换位点(正极)γ-微管蛋白位于中心体外周物质(PCM),用于诱导微管的成核与组装二聚体→原纤丝一个二聚体的β亚基不断加聚到另一个二聚体的α亚基13根原纤丝→片层相邻原纤丝错位1nm,13根形成一个平行四边形微管组装过程(右下图)片层→成核片层弯曲缝合成微管→组装、去组装当一端组装的速
