
《氧化还原反应》PPT说课课件.ppt

yy****24









亲,该文档总共15页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

3氧化还原反应说课 ppt.ppt
3氧化还原反应说课说课人:薛会娟01说教材03说教学目标05说教学方法大家有疑问的,可以询问和交流说教学过程06教学过程四大反应类型06教学过程06教学过程06教学过程06教学过程NaCl的形成过程06教学过程课堂实录06教学过程1.下列反应属于氧化还原反应的是()A.CuO+2HCl====CuCl2+H2OB.CaCO3+2HCl====2NaCl+CO2↑+H2OC.2KMnO4====K2MnO4+MnO2+O2↑D.Ca(OH)2+CO2====CaCO3↓+H2O08教学反思

《氧化还原反应》PPT说课课件.ppt
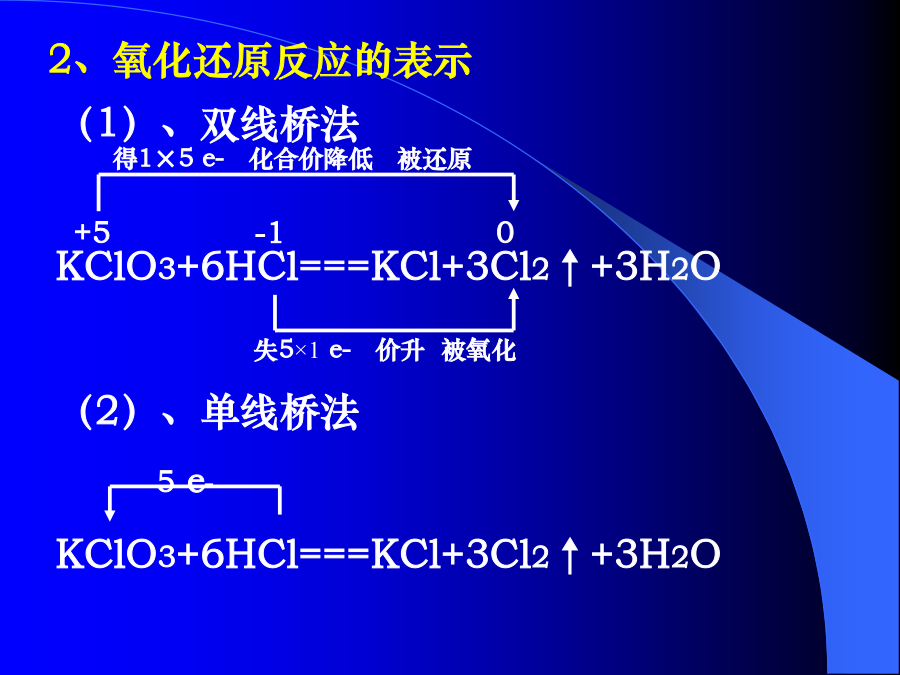
氧化还原反应1、氧化还原反应的概念例1、下列反应中不属于氧化还原反应的是A、3CuS+8HNO3=3Cu(NO3)2+2NO↑+3S↓+4H2OB、3Cl2+6KOH=5KCl+KClO3+3H2OC、Al2(SO4)3+6NaAlO2+12H2O=8Al(OH)3↓+3Na2SO4D、IBr+H2O=HBr+HIO2、氧化还原反应的表示例2、一定条件下硝酸铵受热分解的未配平化学方程式为NH4NO3—HNO3+N2+H2O,在反应中被氧化与被还原的氮原子物质的量之比为()A、1︰1B、5︰4C、5︰3D、

氧化还原反应说课.doc
氧化还原反应资阳中学——曾文中一、教材的地位和作用在中学阶段的基本概念、基础理论知识中,氧化还原反应贯穿于中学化学教材的始终,在是中学化学教学中占有极重要的地位。氧化还原反应是一种常见的化学反应类型,是研究化学反应的一个重要课题。掌握氧化还原反应的知识是学好元素化合物、电化学和元素周期律等知识的重要基础。在大纲中属于C级要求。由于其内容多、涉及面广,思维抽象,它也是中学化学教学的重点和难点所在。氧化还原反应的实际应用也很广泛,可以说我们每个人在工作和生活中都会与氧化还原反应打

氧化还原反应说课.doc
人教版新教材《氧化还原反应》说课各位老师:大家好!今天我给大家说课的内容是人教版必修1第二章第三节《氧化还原反应》。下面我将从教材、学生、教法、教学过程及板书计划五个方面对这节课进行具体分析和阐述。一、说教材1.教材的地位和作用“氧化还原反应”是人教版高一化学新教材第二章第三节的内容。关于氧化还原反应,在中学新课程体系中是分三阶段完成的:在初中阶段从得氧失氧的角度分析理解;在化学必修1中要求在初中化学的基础上,能用化合价升降和电子转移的观点来初步理解氧化还原反应以及了解常见的

氧化还原反应说课.doc
高中化学说课稿:高一化学《氧化还原反应》《氧化还原反应》说课(整节)一教材的地位和作用在中学阶段的基本概念、基础理论知识中,氧化还原反应贯穿于中学化学教材的始终,在是中学化学教学中占有极重要的地位。氧化还原反应是一种常见的化学反应类型,是研究化学反应的一个重要课题。掌握氧化还原反应的知识是学好元素化合物、电化学和元素周期律等知识的重要基础。在中学化学教学大纲中属于C级要求。由于其内容多、涉及面广,思维抽象,它也是中学化学教学的重点和难点所在。氧化还原反应的实际应用也很广泛,可以说我们每个人在工作和生活中都
