
基于造血干细胞为靶细胞的基因治疗.pdf

qw****27







在线预览结束,喜欢就下载吧,查找使用更方便
相关资料

基于造血干细胞为靶细胞的基因治疗.pdf
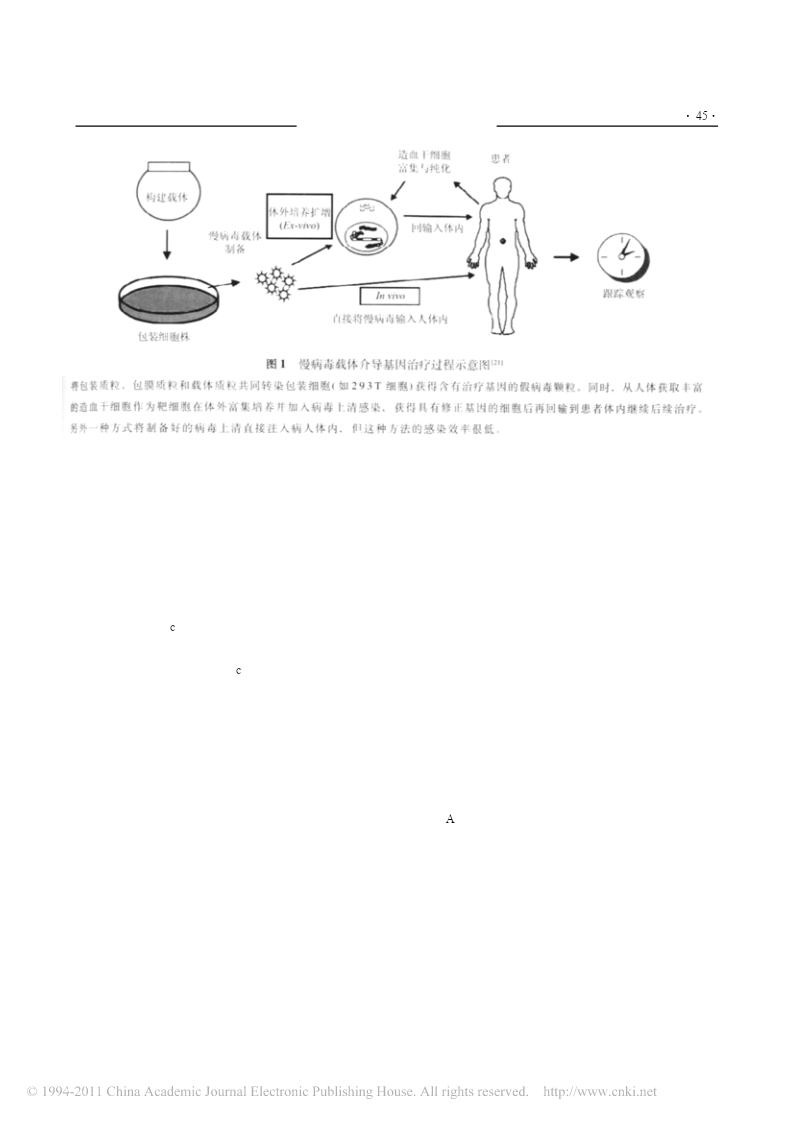
《生命的化学》2011年31卷1期●小综述·41·CHEMISTRYOFLIFE2011,31(1)文章编号:1000-1336(2011)01-0041-08基于造血干细胞为靶细胞的基因治疗张铸业于慧慧王彦刈贵州大学生命科学学院,贵阳550025摘要:在基因治疗中,造血干细胞因为具有自我更新及分化为各种血细胞系的能力而成为一种很有吸引力的靶细胞。将外源目的基因导入造血干细胞,以纠正或补偿因基因缺陷和异常引起的疾病,特别是血液疾病已取得重要进展,例如:腺苷脱氨酶缺陷病、血友病、地中海贫血症及镰状细胞性贫血

日本科学家成功为造血干细胞摄像.pdf
我国科学家发现抑制“过激’’免疫反应

基于HIV--1中和抗体的基因治疗研究.docx
基于HIV--1中和抗体的基因治疗研究基于HIV-1中和抗体的基因治疗研究摘要:艾滋病病毒(HIV)感染目前仍然是全球一项严重的公共卫生问题。在抗逆转录病毒治疗(ART)的帮助下,感染者的生活质量得到了显著改善,但仍然没有可根治的方法。近年来,基因治疗逐渐成为一种潜在的治疗策略。其中,基于HIV-1中和抗体的基因治疗显得尤为重要。本文旨在探索HIV-1中和抗体基因治疗的研究进展和应用前景。引言:HIV-1中和抗体基因治疗是利用生物技术手段将HIV-1中和抗体的基因导入宿主细胞,使其产生中和抗体的特性,从而

造血干细胞与造血干细胞移植.ppt
造血干细胞与造血干细胞移植一、概述(一)造血干细胞(HSC)的起源(二)造血干细胞的表面标志(三)造血微环境(四)造血干细胞的分化二、造血干细胞移植的类别二、造血干/祖细胞移植的原理三、造血干细胞移植的适应证四、HSCT治疗步骤五、HSCT存在问题与展望

造血干细胞及造血干细胞移植.ppt
造血干细胞与造血干细胞移植一、概述(一)造血干细胞(HSC)的起源(二)造血干细胞的表面标志(三)造血微环境(四)造血干细胞的分化二、造血干细胞移植的类别二、造血干/祖细胞移植的原理三、造血干细胞移植的适应证四、HSCT治疗步骤五、HSCT存在问题与展望
