
树突状细胞.ppt

kp****93








亲,该文档总共36页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

树突状细胞.ppt
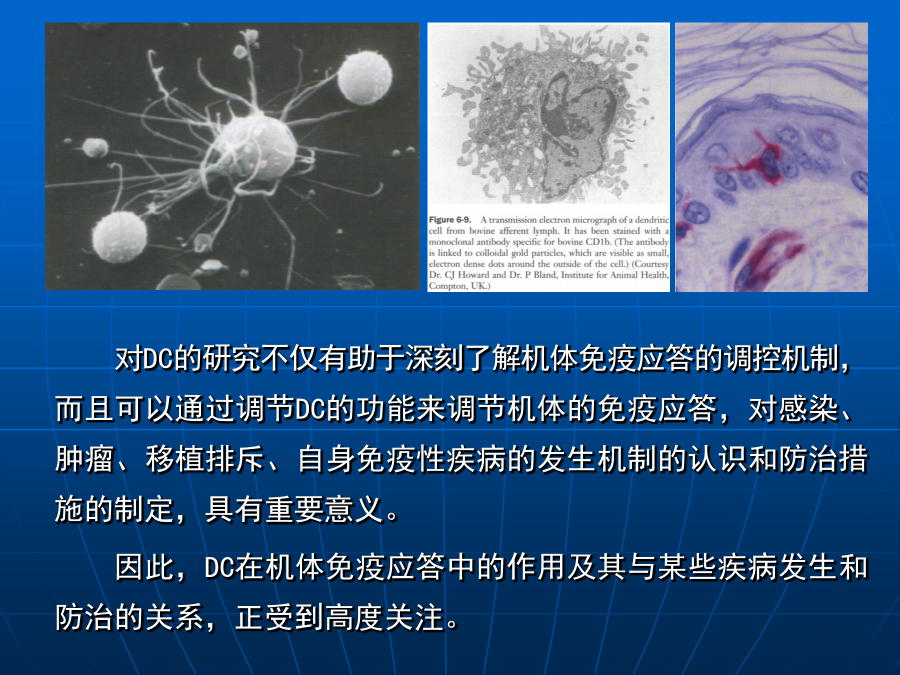
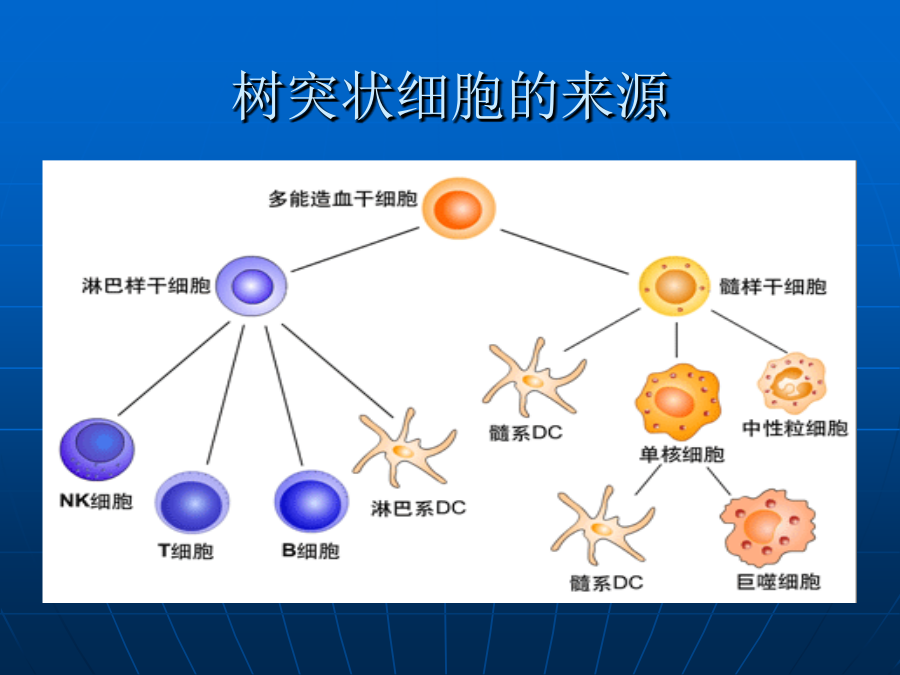
第三讲树突状细胞(dendriticcell,DC)引言对DC的研究不仅有助于深刻了解机体免疫应答的调控机制,而且可以通过调节DC的功能来调节机体的免疫应答,对感染、肿瘤、移植排斥、自身免疫性疾病的发生机制的认识和防治措施的制定,具有重要意义。因此,DC在机体免疫应答中的作用及其与某些疾病发生和防治的关系,正受到高度关注。一、树突状细胞的来源近年研究发现,CD34+HPC在GM-CSF和TNF-α作用下沿三条不同的路线向成熟的DC分化。值得注意的是:CD14+单核细胞分化成的不成熟DC,保留有M-CSF受

树突状细胞0.ppt
资料可以编辑修改使用学习愉快!课件仅供参考哦,实际情况要实际分析哈!感谢您的观看

树突状细胞简介.ppt
讲树突状细胞(dendriticcell,DC)引言对DC的研究不仅有助于深刻了解机体免疫应答的调控机制,而且可以通过调节DC的功能来调节机体的免疫应答,对感染、肿瘤、移植排斥、自身免疫性疾病的发生机制的认识和防治措施的制定,具有重要意义。因此,DC在机体免疫应答中的作用及其与某些疾病发生和防治的关系,正受到高度关注。一、树突状细胞的来源近年研究发现,CD34+HPC在GM-CSF和TNF-α作用下沿三条不同的路线向成熟的DC分化。值得注意的是:CD14+单核细胞分化成的不成熟DC,保留有M-CSF受体。

血液肿瘤树突状细胞.docx
血液肿瘤树突状细胞树突状细胞(DendriticCellsDC)是目前体内功能最强的专职抗原呈递细胞具有启动T细胞介导的免疫反应的功能。本文介绍DC在血液肿瘤中诱导的自身肿瘤杀伤活性、移植免疫、治疗及预后等方面的研究。树突状细胞(DendriticCellsDC)是近年来倍受人们关注的专职抗原呈递细胞(AntigenpresentingCellsAPC)能摄取、加工及呈递抗原启动T细胞介导的免疫反应。DC于1973年首次由Steinman和Cohn发现。近年来关

专职APC树突状细胞.ppt
12345689101112141617骨髓192021222324252627282930
