
铝和铝的化合物.ppt

kp****93








亲,该文档总共33页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

铝和铝的化合物.doc
铝和铝的化合物1.铝在空气中能够稳定存在的原因是()A.铝的活泼性差B.铝的还原性差C.铝与氧气不反应D.铝表面有氧化膜2.氢氧化铝可作为治疗某种胃病的内服药,这是利用了氢氧化铝的哪个性质()A.酸性B.碱性C.两性D.氧化性3.下列物质中既能跟稀H2SO4反应,又能跟氢氧化钠溶液反应的是()①NaHCO3②Al2O3③Al(OH)3④AlA.③④B.②③④C.①③④D.全部4.下列反应的离子方程式书写正确的是()A.钠和冷水反应Na+2H2O=Na++2OH+H2↑B.金属铝溶于氢氧化钠溶液Al+2O

铝和铝的化合物.ppt
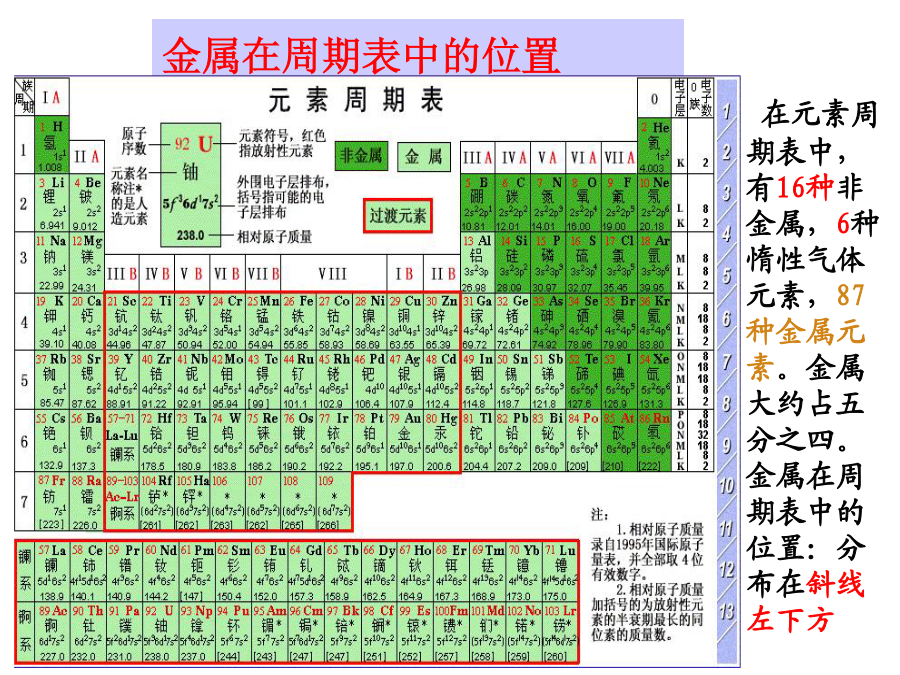
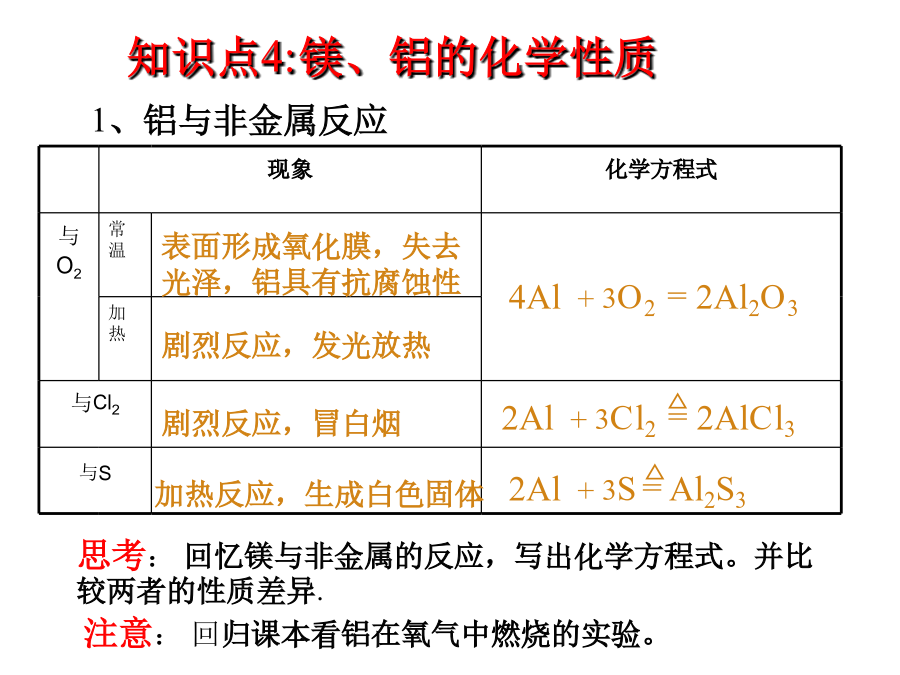
铝及其化合物知识点1:金属概论在元素周期表中,有16种非金属,6种惰性气体元素,87种金属元素。金属大约占五分之四。金属在周期表中的位置:分布在斜线左下方3、概括金属的物理通性:4、金属有何化学共性?试用原子结构知识解释。5、金属的分类:6、合金:知识点2:镁、铝的原子结构知识点3:镁、铝的物理性质知识点4:镁、铝的化学性质2、镁、铝与某些氧化物反应26.粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物。进行如下实验:①取适量A进行铝热反应,产物中有单质B生成;②另取20gA全部溶于0.15L6

铝和铝的化合物.doc
从铝土矿到铝合金班级姓名学号一、选择题:1.最不适宜于制作炊事用具的金属是()A.FeB.ZnC.AlD.Cu2.下列说法正确的是A.所有不锈钢都只含有金属元素B.我国流通的硬币材质是金属单质C.广东打捞的明代沉船上存在大量铝制餐具D.镁合金的硬度和强度均高于纯镁3.有关Al与NaOH溶液的反应的说法中,正确的是()A.铝是还原剂,其氧化产物是Al(OH)3B.NaOH是氧化剂,其还原产物是H2C.铝是还原剂,H2O和NaOH都是氧化剂D.H2O是氧化剂,Al被氧化4.下列关

铝和铝的重要化合物.ppt
铝和铝的化合物二、铝的重要化合物红宝石(Al2O3)红宝石绿宝石蓝宝石(1)氧化铝的物理性质(3)氧化铝的化学性质2、氢氧化铝2、氢氧化铝(2)化学性质(2)化学性质动动脑我们可以运用平衡移动原理做简单分析在Al(OH)3加入酸和碱后,Al(OH)3会以哪种方式电离?加入酸,发生碱式电离,平衡向右移动加入碱,发生酸式电离,平衡向左移动(3)用途知识拓展:3.硫酸铝钾——KAl(SO4)2复盐超强塑性的钛合金材料用于航天航空器的制造归纳与总结练习练习思考

铝和铝的化合物75374.ppt
铝及其化合物知识点1:金属概论在元素周期表中,有16种非金属,6种惰性气体元素,87种金属元素。金属大约占五分之四。金属在周期表中的位置:分布在斜线左下方3、概括金属的物理通性:4、金属有何化学共性?试用原子结构知识解释。5、金属的分类:6、合金:知识点2:镁、铝的原子结构知识点3:镁、铝的物理性质知识点4:镁、铝的化学性质2、镁、铝与某些氧化物反应26.粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物。进行如下实验:①取适量A进行铝热反应,产物中有单质B生成;②另取20gA全部溶于0.15L6
