
一种右兰索拉唑钠的缓释胶囊及其制备方法.pdf

书生****专家










亲,该文档总共22页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料
一种右兰索拉唑钠的缓释胶囊及其制备方法.pdf
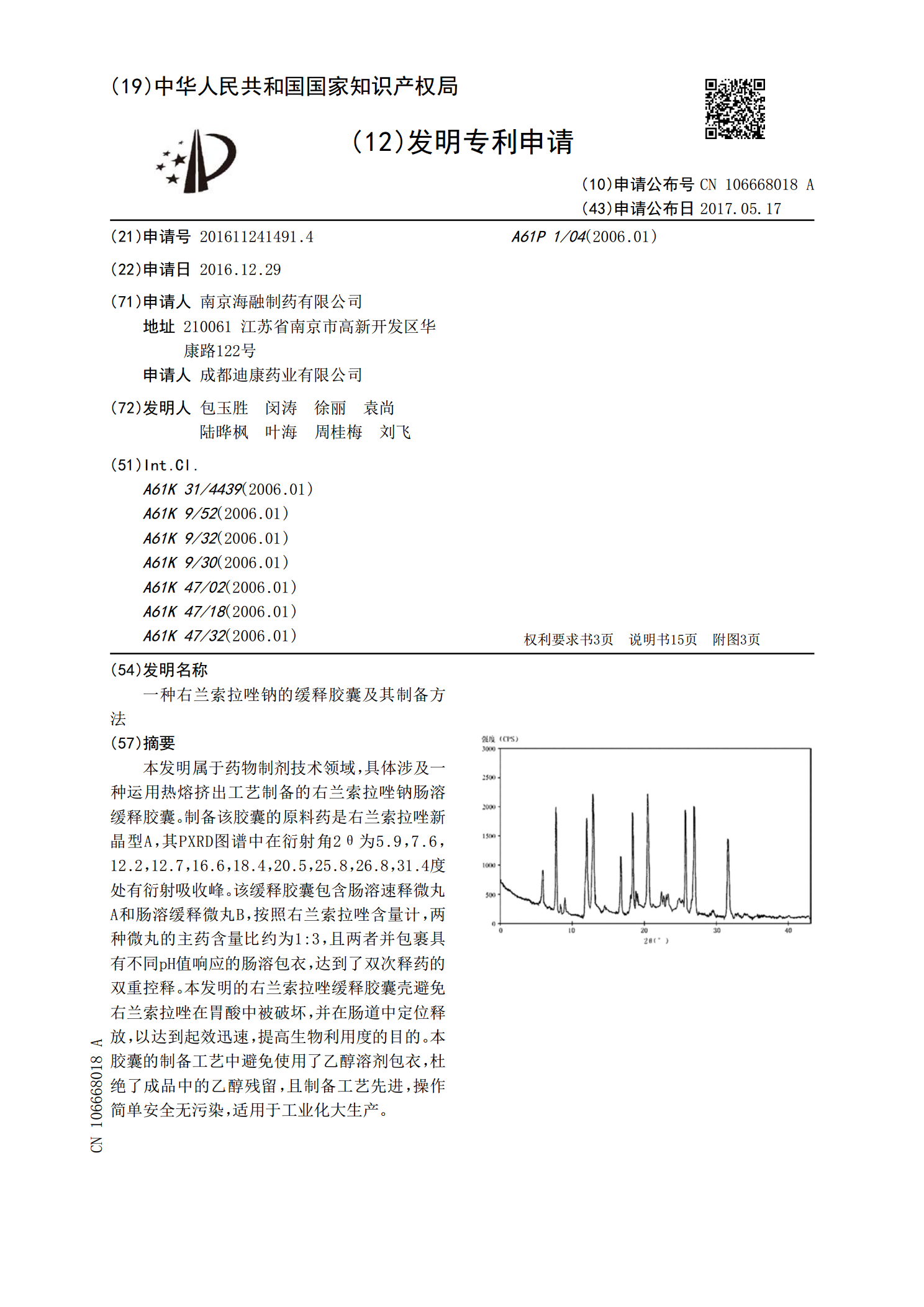
本发明属于药物制剂技术领域,具体涉及一种运用热熔挤出工艺制备的右兰索拉唑钠肠溶缓释胶囊。制备该胶囊的原料药是右兰索拉唑新晶型A,其PXRD图谱中在衍射角2θ为5.9,7.6,12.2,12.7,16.6,18.4,20.5,25.8,26.8,31.4度处有衍射吸收峰。该缓释胶囊包含肠溶速释微丸A和肠溶缓释微丸B,按照右兰索拉唑含量计,两种微丸的主药含量比约为1:3,且两者并包裹具有不同pH值响应的肠溶包衣,达到了双次释药的双重控释。本发明的右兰索拉唑缓释胶囊壳避免右兰索拉唑在胃酸中被破坏,并在肠道中定位

一种右兰索拉唑缓释胶囊及其制备方法.pdf
本发明属于药物制剂技术领域,旨在提高右兰索拉唑在体内的生物利用度。本品在胃酸中几乎不释放,到达肠内才会崩解,使活性成分溶出,从而避免了右兰索拉唑在胃酸中的破坏。本品属于含有2种不同类型的肠溶微丸,从而达到2次释药的双重控释(DDR)。本发明在配制尤特奇S100水分散体过程中,通过加入不同量的碱性物质,中和聚合物中不同摩尔数的羧基,控制肠溶材料在不同的pH值下溶解,从而达到两次释放;采用水分散体包衣,有效避免了乙醇残留。

一种右兰索拉唑缓释制剂及其制备方法与药品.pdf
本发明提供了一种右兰索拉唑缓释制剂及其制备方法与药品,本发明右兰索拉唑缓释制剂具有特定缓释结构,包括基丸,所述基丸外侧依次包覆隔离层和包衣层,所述基丸、隔离层和包衣层分别采用特定成分和用量的原料制备得到,所得右兰索拉唑缓释制剂各类医用药品的制备,尤其适于胶囊型药品的制备,服用后能够广泛、均匀地分布在胃肠道,在胃肠表面分布面积大,从而提高生物利用度、减小或消除药物对胃肠道的刺激,在胃肠道的转运不受食物输送节律、胃排空的影响,释药规律重现性好,流动性较好,有利于制剂分装。本发明右兰索拉唑缓释制剂的制备方法工艺

右兰索拉唑缓释胶囊的研究的任务书.docx
右兰索拉唑缓释胶囊的研究的任务书任务书一、选题背景随着人们生活水平的不断提高,胃肠道疾病的发病率也越来越高,其中包括胃酸过多、胃炎、溃疡等病症。右兰索拉唑是一种常用的胃肠道疾病治疗药物,其主要作用是抑制胃泌酸,从而减轻胃部不适和疼痛。然而,右兰索拉唑通常以片剂的形式出现,且需要口服多次,不太方便使用。因此,开发一种右兰索拉唑缓释胶囊,不仅可以提高药物的使用便捷性,还能够保持药物的疗效。二、研究目的本次研究旨在开发一种右兰索拉唑缓释胶囊,通过对药物的制剂和包装的优化,增加药物的稳定性,提高药物的生物利用度和

一种右兰索拉唑及其制备方法与用途.pdf
本发明提供了一种右兰索拉唑及其制备方法与用途。本发明右兰索拉唑的制备方法通过简单工艺合成右兰索拉唑粗品,通过进一步的光学纯度精制和提纯能够得到光学纯度近100%的高纯度的右兰索拉唑产品。本发明右兰索拉唑产品光学纯度近100%,纯度高,能够用做药用成分,具有更好的效果。
