
1第二节物质的量的单位第3课时.ppt

qw****27








亲,该文档总共28页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

1第二节物质的量的单位第3课时.ppt
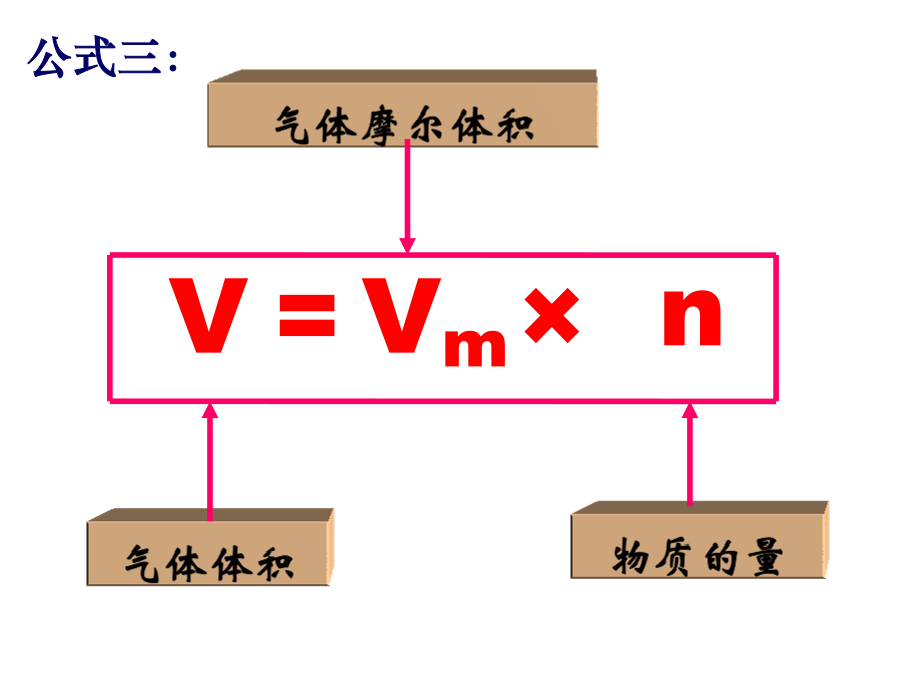
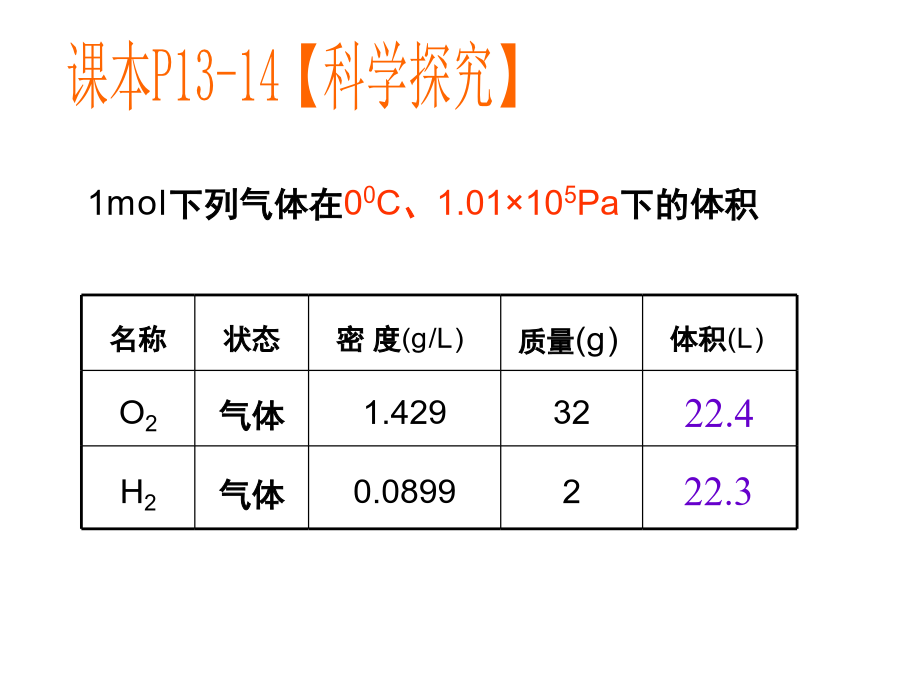
第一章第二节第3课时气体摩尔体积定义:单位物质的量的气体所占的体积叫做气体摩尔体积。气体摩尔体积1mol物质体积相同吗???1mol下列气体在00C、1.01×105Pa下的体积1mol气体在00C、1.01×105Pa下的体积在相同条件下,等物质的量(如1mol)固体或液体的体积一般各不相同,但气体的体积却大致相同。物体体积大小取决于什么因素呢?1.粒子数目2.粒子的大小3.粒子之间的距离学习探究:阅读课本14页,了解:学习小结:学习小结:22.4L(标准状况)例题:1、在标准状况下,2.2gCO2的体

1第二节物质的量的单位第2课时.ppt
高中化学必修1物质的量的单位—摩尔物质的量的单位—摩尔一、课前复习:一、物质的量的单位—摩尔一、物质的量的单位—摩尔二、摩尔质量二、摩尔质量例:再见!

第1课时物质的量的单位——摩尔.ppt
第二节化学计量在实验中的应用看Flash,思考:物质由哪些微粒组成?该如何称量?1.了解物质的量、摩尔质量的概念、单位(重点)2.理解阿伏加德罗常数的含义(难点)3.掌握物质的量与微观粒子之间的简单换算关系(重点)铅笔是一打一打的根据上面的图例,联系生活中的计量方法,请思考下面的问题:对于细小的物品,用打、排、盒等来计量有哪些好处?打、排、盒和只有怎样的数量关系?1.不同的物质可能有不同的计量方法。(方便)化学反应是原子、离子或分子之间按一定的数目关系进行的。对于原子、离子和分子等我们不仅直接用肉眼看不到

第1课时物质的量的单位——摩尔.ppt
第二节化学计量在实验中的应用世界是物质的,物质由哪些微粒组成?该如何称量?观看Flash,认真的体会。一打=12支原子、离子和分子等不仅我们直接用肉眼看不到,也难以称量。用什么方法来计量原子、离子或分子(外观较小)呢?微观粒子个体很小,当数量很大时,我们将以集团(集体)为单位对其进行计量。一、物质的量(n)表示含有一定数目粒子的集合体的物理量。符号为n。单位为“摩尔”符号为mol物理量国际上规定,1mol粒子集合体所含的粒子数与0.012kg12C中所含的碳原子数相同。0.012kg12C中所含的碳原子数

第1课时物质的量的单位——摩尔.ppt
第二节化学计量在实验中的应用铅笔是一打一打的根据上面的图例,联系生活中的计量方法,请思考下面的问题:对于细小的物品,用打、排、盒等来计量有哪些好处?打、排、盒和只有怎样的数量关系?一、物质的量(n)表示含有一定数目粒子的集合体的物理量。符号为n。单位为“摩尔”,单位符号为mol。【练一练】【提示】国际上规定,1mol粒子集合体所含的粒子数与0.012kg12C中所含的碳原子数相同,约为6.02×1023。把1mol任何粒子的粒子数叫做阿伏伽德罗常数,通常用6.02×1023mol-1=在0.5molO2中
