
水的电离电解质在水溶液中的存在形态.ppt

仙人****88









在线预览结束,喜欢就下载吧,查找使用更方便
相关资料

水的电离电解质在水溶液中的存在形态.ppt
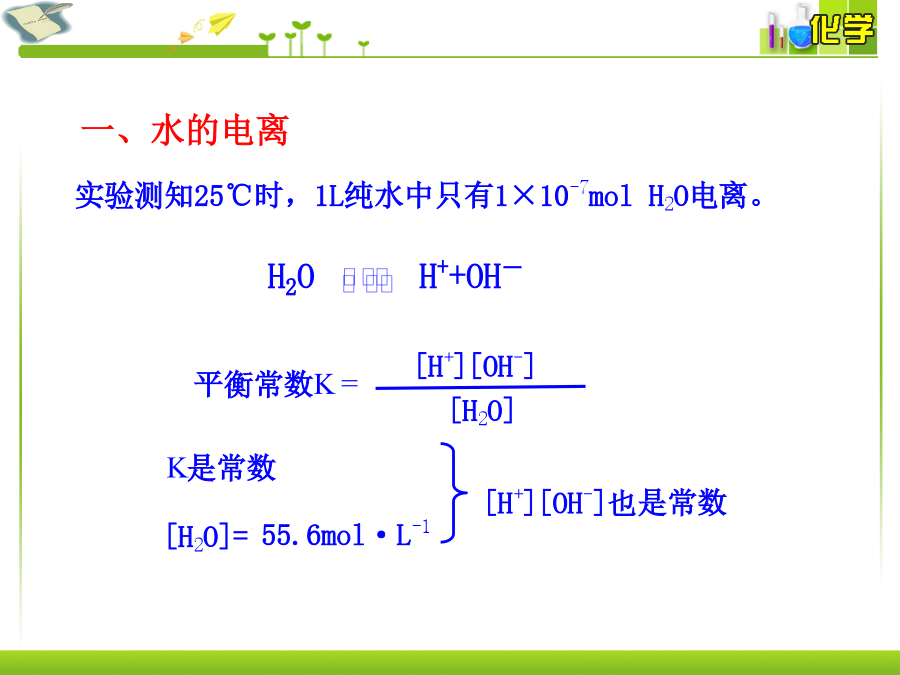
第3章物质在水溶液中的行为第1节水溶液水的电离精确的实验证明,纯水能导电。纯水能微弱电离出H+和OH-,水是一种极弱的电解质。水的电离方程式:平衡常数K=水的离子积KW=[H+][OH-]室温下,0.1mol·L-1的盐酸中,水电离出的[H+]是多少?水电离出的[OH-]呢?25℃时,0.1mol·L-1的NaOH溶液中,c(OH-)=?c(H+)=?水电离出的c(OH-)水=?c(H+)水=?常温下,水电离出的[H+]为10-13mol•L-1时,溶液是酸溶液,还是碱溶液?1.水的离子积常数KW,简称水

电解质在水溶液中的存在形态.ppt
第三章水溶液一、电解质与非电解质二、强电解质与弱电解质课堂练习:三、电解质的电离方程式课堂练习:

高中化学物质在水溶液中的行为水溶液时水的电离电解质在水溶液中的存在形态鲁科学习.pptx
会计学过程与方法:能运用化学平衡的理论处理水溶液中的问题,进一步树立平衡观和离子观的思想,并掌握从简单到复杂、从单一研究对象到多个研究对象的对复杂体系的研究方法。情感态度与价值观:认识调控溶液pH在工农业生产和科学研究中的重要应用;能通过实例认识盐类水解在生产、生活中的应用;通过酸碱中和滴定等活动,体会定量的方法在科学研究中的作用。第1节水溶液第1课时水的电离电解质在水溶液中的存在形态1.理解水的电离过程以及水的离子积常数的含义,并能应用水的离子积常数进行相关计算。2.知道强弱电解质的区别,理解弱电解质的

高中化学 第三章 物质在水溶液中的行为 3.1.1 水的电离 电解质在水溶液中的存在形态课件 鲁科版.pptx
第3章物质在水溶液中的行为第1节水溶液第1课时水的电离电解质在水溶液中的存在形态一一一一一一探究一探究一探究一探究一探究一探究一探究一探究一探究一探究一探究一探究一探究一探究一1234512345123451234512345

电解质在水溶液中的存在形态PPT课件.ppt
第三章水溶液一、电解质与非电解质二、强电解质与弱电解质课堂练习:三、电解质的电离方程式课堂练习:
