
原电池电极的判断方法.pptx

仙人****88







在线预览结束,喜欢就下载吧,查找使用更方便
相关资料

原电池电极的判断方法.pptx
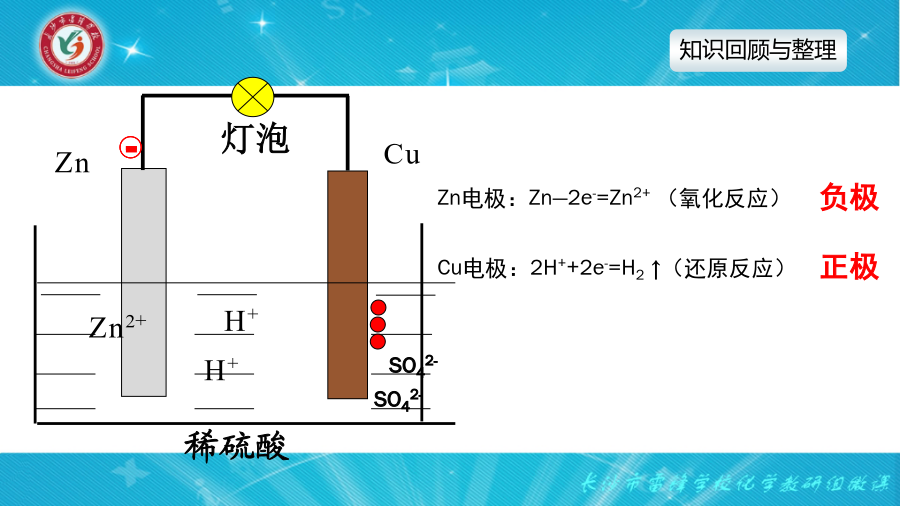
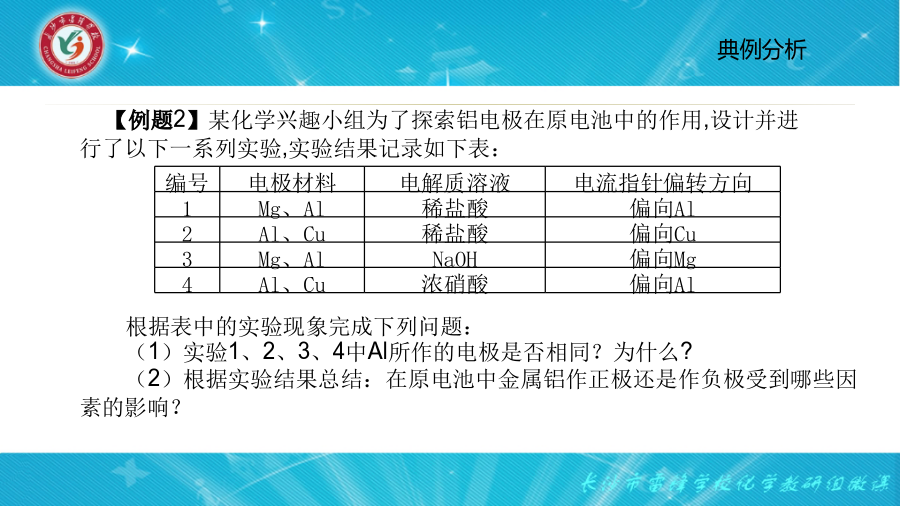
课题:原电池电极的判断方法通过本课的学习,能多角度理解原电池正极和负极的判断方法。编号解析:实验1中Mg,Al均可与稀盐酸自发发生氧化还原反应,但Mg更活泼,故Mg作负极;实验2中Al可与稀盐酸自发发生氧化还原反应,Cu不反应,故Al作负极;实验3中Mg虽比Al活泼,但Mg不能与NaOH溶液反应,而Al可与NaOH溶液反应,故Al作负极;实验4中Al虽比Cu活泼,但常温下,Al遇浓硝酸发生钝化,阻止内部的金属继续与酸反应,而Cu与浓硝酸可自发反应,故Cu作负极。由以上4组实验,可总结出金属铝在原电池中作正

原电池电极的判断方法(梁)(1).pptx
课题:原电池电极的判断方法通过本课的学习,能多角度理解原电池正极和负极的判断方法。编号解析:实验1中Mg,Al均可与稀盐酸自发发生氧化还原反应,但Mg更活泼,故Mg作负极;实验2中Al可与稀盐酸自发发生氧化还原反应,Cu不反应,故Al作负极;实验3中Mg虽比Al活泼,但Mg不能与NaOH溶液反应,而Al可与NaOH溶液反应,故Al作负极;实验4中Al虽比Cu活泼,但常温下,Al遇浓硝酸发生钝化,阻止内部的金属继续与酸反应,而Cu与浓硝酸可自发反应,故Cu作负极。由以上4组实验,可总结出金属铝在原电池中作正

原电池电极判断及相关现象分析.docx
精选资料可修改编辑“电化学”板块是化学高考中的必考内容,多以选择题形式出现,亦或参杂在后边的解答题中一起考察,考察分数为6——8分。所以“电化学”的学习,一直是高中化学的重点内容。今天,大家一起梳理下高一化学必修二中“原电池”的相关内容和考点,以便更好的掌握这一部分内容。一、构成原电池的基本条件1、活泼型不同的两个电极2、可以自发进行氧化还原反应3、形成闭合回路4、有电解质溶液二、原电池电极极性的判断01根据电极材料判断一般情况下,活泼性强的金属为负极,活泼性较弱的金属或导电的非金属为正极。02根据电极反

原电池电极反应式的书写方法.ppt
主讲人:詹忠国谢谢!

电解池电极的判断方法.ppt
电解池电极的判断方法
