
【全程复习方略】2013版中考化学 第3章 物质构成的奥秘 第1节 构成物质的基本微粒配套课件 沪教版.ppt

努力****星驰










亲,该文档总共50页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

【全程复习方略】2013版中考化学 第3章 物质构成的奥秘 第1节 构成物质的基本微粒配套课件 沪教版.ppt
第1节构成物质的基本微粒微粒的性质1.物质都是由肉眼看不见的微粒构成的构成物质的基本微粒有_____、_____和_____。2.微粒的性质(1)其_____和_____都很小;(2)微粒是不断_____的且温度越高微粒的运动速率_____。(3)微粒之间有一定的_____。①空隙大小与温度、压强的关系温度_____压强_____空隙越小。②空隙大小与物质状态的关系气体中微粒之间的空隙>液体中微粒之间的空隙>固体微粒之间的空隙。【思考感悟】“物质的热胀冷缩现象是由于温度发
【全程复习方略】2013版中考化学 第3章 物质构成的奥秘 第1节 构成物质的基本微粒精练精析 沪教版.doc
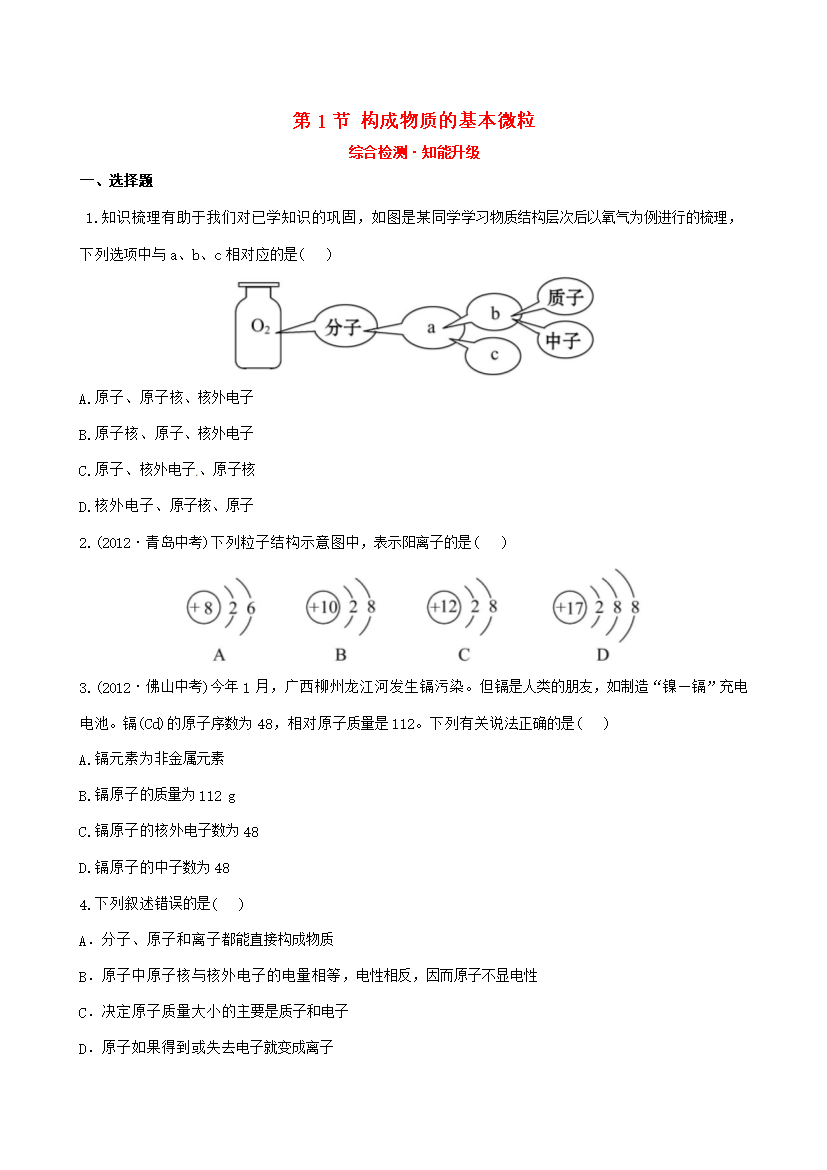
第1节构成物质的基本微粒综合检测·知能升级一、选择题1.知识梳理有助于我们对已学知识的巩固如图是某同学学习物质结构层次后以氧气为例进行的梳理下列选项中与a、b、c相对应的是()A.原子、原子核、核外电子B.原子核、原子、核外电子C.原子、核外电子、原子核D.核外电子、原子核、原子2.(2012·青岛中考)下列粒子结构示意图中表示阳离子的是()3.(2012·佛山中考)今年1月广西柳州龙江河发生镉污染。但镉是人类的朋友如制造“镍—镉”充电电池。镉(Cd)的原子序数为48相对原子质量是112。

【全程复习方略】2013版中考化学 第3章 物质构成的奥秘 第1节 构成物质的基本微粒精练精析 沪教版.doc
第1节构成物质的基本微粒综合检测·知能升级一、选择题1.知识梳理有助于我们对已学知识的巩固,如图是某同学学习物质结构层次后以氧气为例进行的梳理,下列选项中与a、b、c相对应的是()A.原子、原子核、核外电子B.原子核、原子、核外电子C.原子、核外电子、原子核D.核外电子、原子核、原子2.(2012·青岛中考)下列粒子结构示意图中,表示阳离子的是()3.(2012·佛山中考)今年1月,广西柳州龙江河发生镉污染。但镉是人类的朋友,如制造“镍—镉”充电电池。镉(Cd)的原子序数为48,相对原子质量是112。下列

【全程复习方略】2013版中考化学 第3章 物质构成的奥秘 第2节 物质的组成及表示配套课件 沪教版.ppt
第2节物质的组成及表示组成物质的化学元素1.元素和元素符号(1)元素:①概念:具有相同_________(即_______)的同一类原子的总称。②分类:分为_________、___________、_____________三大类。(2)元素符号:①书写用1个或2个拉丁字母表示第一个字母_____第二个字母_____。②意义a.宏观:表示_________。b.微观:表示___________________。如H:宏观表示_______;微观表示__________

课件-全国-2014_2013版中考化学 第3章 物质构成的奥秘 第1节 构成物质的基本微粒配套课件 沪教版.rar
第1节构成物质的基本微粒微粒的性质1.物质都是由肉眼看不见的微粒构成的,构成物质的基本微粒有_____、_____和_____。2.微粒的性质(1)其_____和_____都很小;(2)微粒是不断_____的,且温度越高,微粒的运动速率_____。(3)微粒之间有一定的_____。①空隙大小与温度、压强的关系温度_____,压强_____,空隙越小。②空隙大小与物质状态的关系气体中微粒之间的空隙>液体中微粒之间的空隙>固体微粒之间的空隙。【思考感悟】“物质的热胀冷缩现象是由于温度发生改变时,微粒体积发生改
