
金属晶体堆积模型及计算.ppt

仙人****88










亲,该文档总共33页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料
金属晶体堆积模型及计算.ppt
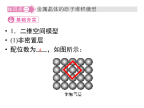
1.二维空间模型(1)非密置层配位数为,如图所示:(2)密置层配位数为,如图所示:2.三维空间模型(1)非密置层在三维空间堆积①简单立方堆积相邻非密置层原子的原子核在的堆积,空间利用率太低,只有金属采用这种堆积方式。1、简单立方堆积②体心立方堆积将上层金属原子填入下层的金属原子形成的凹穴中,并使非密置层的原子稍稍分离。这种堆积方式所得的晶胞是一个含有两个原子的立方体,一个原子在立方体的,另一个原子在立方体的,其空间的利用率比简单立方堆积高,碱金属属于这种堆积方式。配位数:(2)密置层在三维空间堆积①六方最

金属晶体堆积模型及计算.ppt
第三节金属晶体1、金属键的定义:金属离子和自由电子之间的强烈的相互作用,叫金属键。(1)金属键的成键微粒是金属阳离子和自由电子。(2)金属键存在于金属单质和合金中。(3)金属键没有方向性也没有饱和性。二、电子气理论经典的金属键理论叫做“电子气理论”。它把金属键形象地描绘成从金属原子上“脱落”下来的价电子形成遍布整块晶体的“电子气”,被所有原子所共用,从而把所有金属原子维系在一起。金属晶体也是巨分子。电子气理论对金属的物理性质的解释物质“电子气”(自由电子)在热的作用下与金属原子频繁碰撞从而把能量从温度高的
金属晶体堆积模型及计算.ppt
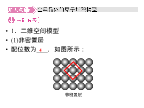
1.二维空间模型(1)非密置层配位数为,如图所示:(2)密置层配位数为,如图所示:2.三维空间模型(1)非密置层在三维空间堆积①简单立方堆积相邻非密置层原子的原子核在的堆积,空间利用率太低,只有金属采用这种堆积方式。1、简单立方堆积②体心立方堆积将上层金属原子填入下层的金属原子形成的凹穴中,并使非密置层的原子稍稍分离。这种堆积方式所得的晶胞是一个含有两个原子的立方体,一个原子在立方体的,另一个原子在立方体的,其空间的利用率比简单立方堆积高,碱金属属于这种堆积方式。(2)钾型配位数:(2)密置层在三维空间堆

金属晶体堆积模型及计算课程.pptx
金属晶体堆积模型及计算1、下列生活中的问题,不能用金属键知识解释的是()A、用铁制品做炊具B、用金属铝制成导线C、用铂金做首饰D、铁易生锈回顾练习3、金属键的强弱与金属价电子数的多少有关,价电子数越多金属键越强;与金属阳离子的半径大小也有关,金属阳离子的半径越大,金属键越弱。据此判断下列金属熔点逐渐升高的是()A、LiNaKB、NaMgAlC、LiBeMgD、LiNaMg回顾练习一、金属晶体的原子堆积模型2、二维堆积3、三维堆积这种堆积晶胞是一个体心立方,每个晶胞每个晶胞含个原子,空间利用率不高(68%)

金属晶体堆积模型及计算ppt课件.ppt
第三节金属晶体1、下列生活中的问题,不能用金属键知识解释的是()A、用铁制品做炊具B、用金属铝制成导线C、用铂金做首饰D、铁易生锈回顾练习3、金属键的强弱与金属价电子数的多少有关,价电子数越多金属键越强;与金属阳离子的半径大小也有关,金属阳离子的半径越大,金属键越弱。据此判断下列金属熔点逐渐升高的是()A、LiNaKB、NaMgAlC、LiBeMgD、LiNaMg回顾练习一、金属晶体的原子堆积模型2、二维堆积3、三维堆积(1).简单立方堆积:(2)钾型这种堆积晶胞是一个体心立方,每个晶胞每个晶胞含个原子,
