
高中化学:2.3.1《化学能与电能的转化》学案 (苏教版必修2).doc

小新****ou






在线预览结束,喜欢就下载吧,查找使用更方便
相关资料

高中化学:2.3.1《化学能与电能的转化》学案 (苏教版必修2).doc
《化学能与电能的转化》学案第一课时化学能转化为电能【学习目标】1.初步认识原电池的原理和一般构成条件;2.培养学生的实验操作能力、观察能力、科学的学习方法和创造性思维和探究能力以及提出问题、分析问题和解决问题的能力;3.应用辩证唯物主义的思维方法抓住氧化还原反应是原电池工作原理的本质。通过实验不断体现出由实践—认识—再实践—再认识的认知过程。【知识梳理】一、化学能转化为电能(一)原电池原理探究【活动探究】分组进行下列实验并完
高中化学:2.3.1 化学能与电能的转化 学案 苏教版必修2.doc
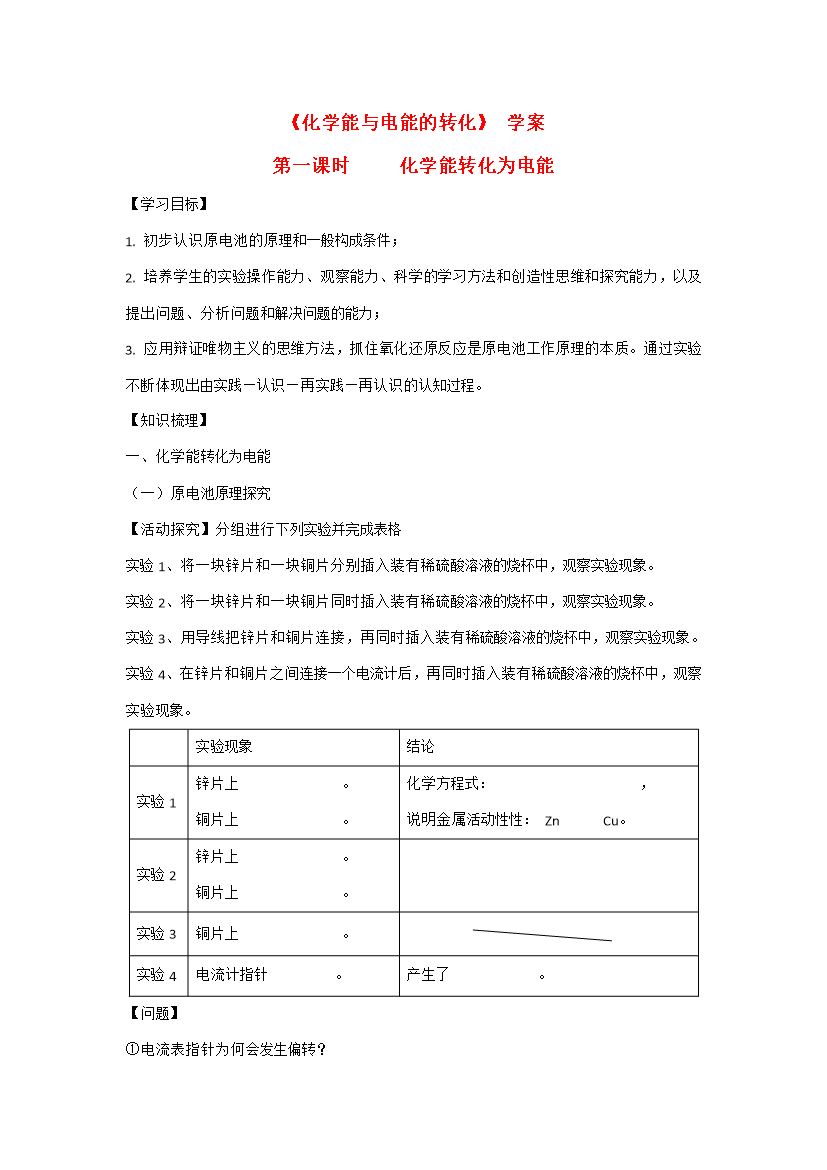
《化学能与电能的转化》学案第一课时化学能转化为电能【学习目标】1.初步认识原电池的原理和一般构成条件;2.培养学生的实验操作能力、观察能力、科学的学习方法和创造性思维和探究能力以及提出问题、分析问题和解决问题的能力;3.应用辩证唯物主义的思维方法抓住氧化还原反应是原电池工作原理的本质。通过实验不断体现出由实践—认识—再实践—再认识的认知过程。【知识梳理】一、化学能转化为电能(一)原电池原理探究【活动探究】分组进行下列实验并完成表格实验1、将一块锌片和一块铜片分别插入装有稀硫酸溶液的烧杯中

高中化学:2.3《化学能与电能的转化》学案苏教版必修2.doc
第三单元:化学能与电能的转化第一课时一、教学目标课标内容:1.体验化学能与电能相互转化和探究过程了解原电池和电解池的工作原理能写出电极反应和电池反应方程式2.认识化学能与电能相互转化的实际意义及其重要作用会考考纲:1.举例说明化学能与电能的转化关系及其应用(A)2.通过制作简易原电池的实验了解原电池的概念和原理(B)3.认识高能燃料的燃烧效率、开发高能清洁燃料和研制新型电池的重要作用(BⅡ)教学目标:(一)知识与技能1.通过实例了解常见的化学能与电能的转化方式2.理解原电池的工作原理掌握原电池的构成条件正

高中化学:2.3.2 化学能与电能的转化 学案苏教版必修2.doc
《第三节化学能与电能的转化》学案第二课时化学电源【学习目标】1.认识化学电源的分类及常见的化学电源;2.了解废旧电池的处理培养可持续发展的环保意识。【知识梳理】化学电源一、化学电源的分类化学电源分类实例特点及应用一次电池二次电池燃料电池思考:如何根据电池反应判断电极性质?名称放电反应负极锌锰电池Zn+2MnO2+2NH4Cl=ZnCl2+2MnO(OH)+2NH3锌汞电池Zn+HgO+H2O=Zn(OH)2+Hg铅蓄电池Pb+PbO2+2H2SO4═2
高中化学:2.3.3《化学能与电能的转化》学案(苏教版必修2).doc
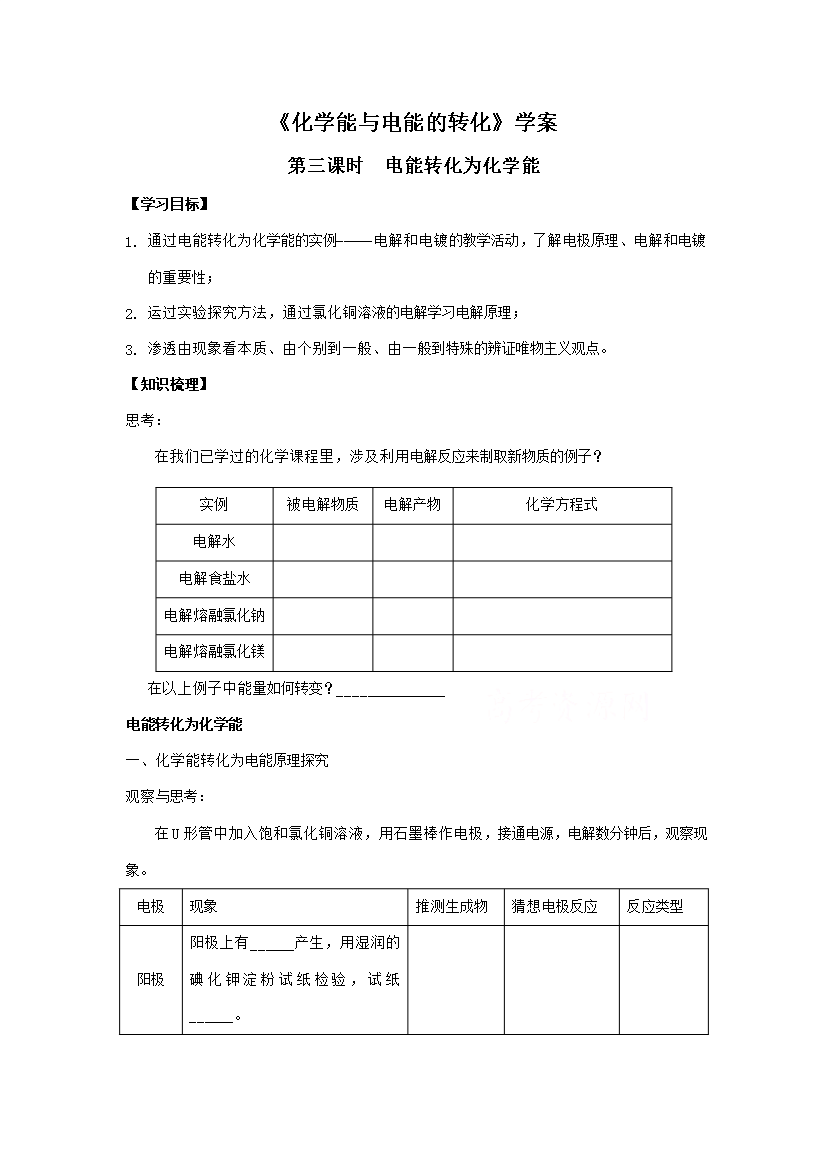
《化学能与电能的转化》学案第三课时电能转化为化学能【学习目标】1.通过电能转化为化学能的实例-----电解和电镀的教学活动了解电极原理、电解和电镀的重要性;2.运过实验探究方法通过氯化铜溶液的电解学习电解原理;3.渗透由现象看本质、由个别到一般、由一般到特殊的辨证唯物主义观点。【知识梳理】思考:在我们已学过的化学课程里涉及利用电解反应来制取新物质的例子?实例被电解物质电解产物化学方程式电解水电解食盐水电解熔融氯化钠电解熔融氯化镁在以上例子中能量如何转变?___________
