
高考化学二轮复习 专题七 电化学专题测试 新人教版新-新人教版高三全册化学试题.doc

鹏飞****可爱









在线预览结束,喜欢就下载吧,查找使用更方便
相关资料

高考化学二轮复习 专题七 电化学专题测试 新人教版新-新人教版高三全册化学试题.doc
专题七电化学1.下列金属防护的方法不正确的是()A.对健身器材涂油漆以防止生锈B.对某些工具的“机械转动部位”选用刷油漆的方法来防锈C.用牺牲锌块的方法来保护船身D.自行车的钢圈上镀上一层铬防锈【答案】B【解析】B项中应选用润滑油来达到润滑和防锈的目的。2.下图所示的日常生活装置中与手机充电时的能量转化形式相同的是()【答案】A【解析】A项是将电能转化成化学能;B项是将水的势能转化成电能;C项是将太阳能转化成热能;D项是将化学能转化成电能。3.下列有关电化学的示意图中正确的是()【答案】D

高考化学二轮复习 专题七 电化学专题测试 新人教版新-新人教版高三全册化学试题.doc
专题七电化学1.下列金属防护的方法不正确的是()A.对健身器材涂油漆以防止生锈B.对某些工具的“机械转动部位”选用刷油漆的方法来防锈C.用牺牲锌块的方法来保护船身D.自行车的钢圈上镀上一层铬防锈【答案】B【解析】B项中应选用润滑油来达到润滑和防锈的目的。2.下图所示的日常生活装置中,与手机充电时的能量转化形式相同的是()【答案】A【解析】A项是将电能转化成化学能;B项是将水的势能转化成电能;C项是将太阳能转化成热能;D项是将化学能转化成电能。3.下列有关电化学的示意图中正确的是()【答案】D【解析】选项A

高考化学二轮复习 专题七 电化学专题复习 新人教版-新人教版高三全册化学试题.doc
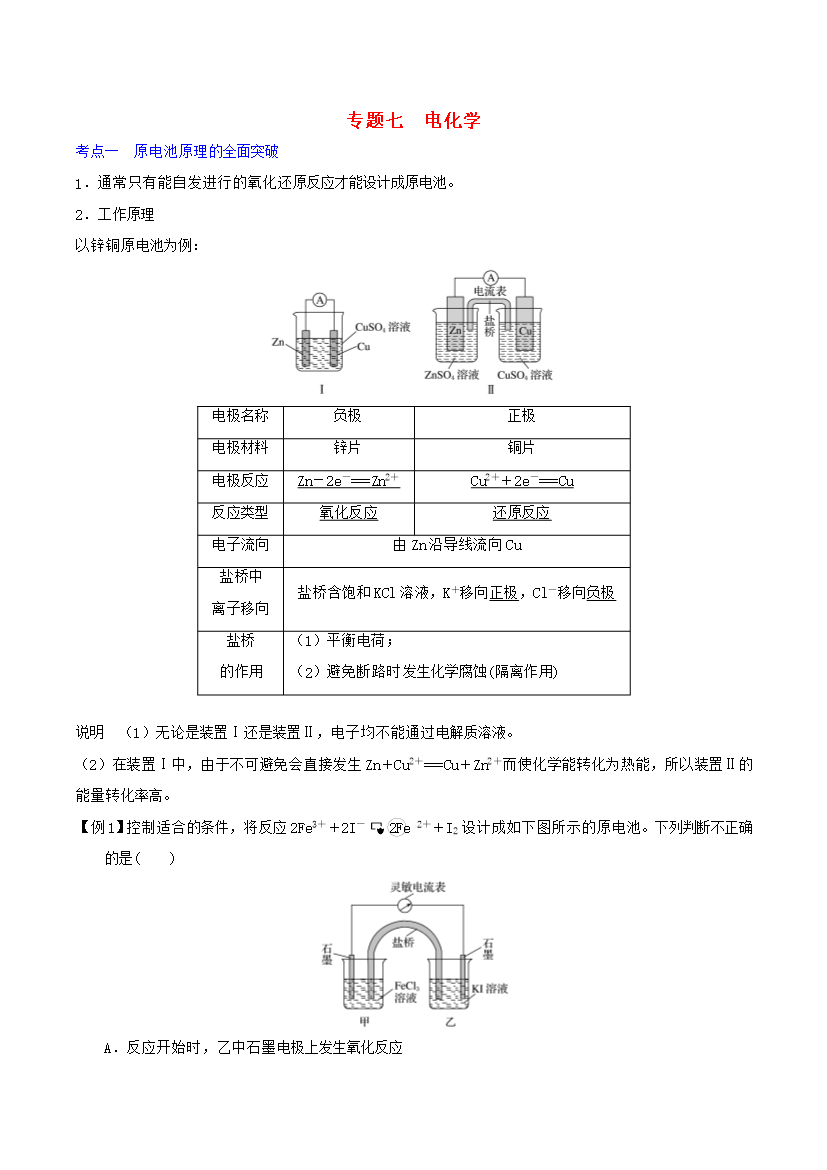
专题七电化学考点一原电池原理的全面突破1.通常只有能自发进行的氧化还原反应才能设计成原电池。2.工作原理以锌铜原电池为例:电极名称负极正极电极材料锌片铜片电极反应Zn-2e-===Zn2+Cu2++2e-===Cu反应类型氧化反应还原反应电子流向由Zn沿导线流向Cu盐桥中离子移向盐桥含饱和KCl溶液,K+移向正极,Cl-移向负极盐桥的作用(1)平衡电荷;(2)避免断路时发生化学腐蚀(隔离作用)说明(1)无论是装置Ⅰ还是装置Ⅱ,电子均不能通过电解质溶液。(2)在装置Ⅰ中,由于不可避免会直接发生Zn+Cu2+
高考化学二轮复习 专题七 电化学专题复习 新人教版-新人教版高三全册化学试题.doc
专题七电化学考点一原电池原理的全面突破1.通常只有能自发进行的氧化还原反应才能设计成原电池。2.工作原理以锌铜原电池为例:电极名称负极正极电极材料锌片铜片电极反应Zn-2e-===Zn2+Cu2++2e-===Cu反应类型氧化反应还原反应电子流向由Zn沿导线流向Cu盐桥中离子移向盐桥含饱和KCl溶液K+移向正极Cl-移向负极盐桥的作用(1)平衡电荷;(2)避免断路时发生化学腐蚀(隔离作用)说明(1)无论是装置Ⅰ还是装置Ⅱ电子均不能通过电解质溶液。(2)在装置Ⅰ中由于不可避免会直接发生Zn+Cu2+

高考化学二轮专题复习 专题七 电化学限时集训-人教版高三全册化学试题.doc
专题七电化学1.江苏正在建设世界最大的海上风电场,防腐蚀是建设海上风电场需要特别注意的问题,下列说法正确的是()A.海水的pH一般在8.0~8.5之间,对风电机钢铁支架的腐蚀主要是析氢腐蚀B.腐蚀总反应4Fe+3O2+2xH2O2[Fe2O3·xH2O](铁锈)的ΔH>0,ΔS<0C.钢部件镀锌前,可用碱液洗去表面的铁锈D.热喷涂锌铝合金,可以减缓管道的腐蚀2.普通电解精炼铜的方法所制备的铜中仍含杂质,利用如图Z7-1中的双膜(阴离子交换膜和过滤膜)电解装置可制备高纯度的Cu。下列有关叙述正确的是()图Z
