
课堂新概念高考化学一轮复习 27原电池 化学电源练习-人教版高三全册化学试题.doc

元枫****文章










亲,该文档总共12页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

课堂新概念高考化学一轮复习 27原电池 化学电源练习-人教版高三全册化学试题.doc
原电池化学电源A组双基题组1.(选修4P78T3)镉镍可充电电池在现代生活中有广泛应用它的充、放电反应按下式进行:Cd+2NiOOH+2H2OCd(OH)2+2Ni(OH)2由此可知该电池放电时的负极是()A.Cd(OH)2B.Ni(OH)2C.CdD.NiOOH【解析】充电电池的放电过程为原电池原理故该反应是从左到右被氧化的是Cd作负极。【答案】C2.(2014·合肥市高三二检)镁及其化合物一般无毒(或低毒)、无污染且镁电池放电时电压高而平稳。其中一种镁电池的反应为xMg+M

课堂新概念高考化学一轮复习 27原电池 化学电源练习-人教版高三全册化学试题.doc
原电池化学电源A组双基题组1.(选修4P78T3)镉镍可充电电池在现代生活中有广泛应用,它的充、放电反应按下式进行:Cd+2NiOOH+2H2OCd(OH)2+2Ni(OH)2由此可知,该电池放电时的负极是()A.Cd(OH)2B.Ni(OH)2C.CdD.NiOOH【解析】充电电池的放电过程为原电池原理,故该反应是从左到右,被氧化的是Cd,作负极。【答案】C2.(2014·合肥市高三二检)镁及其化合物一般无毒(或低毒)、无污染,且镁电池放电时电压高而平稳。其中一种镁电池的反应为xMg+Mo3S4MgxM

课堂新概念高考化学一轮复习 27原电池 化学电源讲义-人教版高三全册化学试题.doc
原电池化学电源1.了解原电池的工作原理能写出电极反应和电池反应方程式。(高频)2.了解常见的化学电源的种类及其工作原理。(中频)原电池1.概念:把化学能转化为电能的装置。2.工作原理:(以铜—锌原电池为例)单液原电池双液原电池装置图电极名称负极正极电极材料锌片铜片电极反应Zn-2e-===Zn2+Cu2++2e-===Cu反应类型氧化反应还原反应电子流向由锌片沿导线方向流向铜片电池反应方程式Zn+Cu2+===Zn2++Cu不同点Zn在CuSO4溶液中直接接触Cu2+会有一部分Zn与Cu2+直接反应该

课堂新概念高考化学一轮复习 27原电池 化学电源讲义-人教版高三全册化学试题.doc
原电池化学电源1.了解原电池的工作原理,能写出电极反应和电池反应方程式。(高频)2.了解常见的化学电源的种类及其工作原理。(中频)原电池1.概念:把化学能转化为电能的装置。2.工作原理:(以铜—锌原电池为例)单液原电池双液原电池装置图电极名称负极正极电极材料锌片铜片电极反应Zn-2e-===Zn2+Cu2++2e-===Cu反应类型氧化反应还原反应电子流向由锌片沿导线方向流向铜片电池反应方程式Zn+Cu2+===Zn2++Cu不同点Zn在CuSO4溶液中直接接触Cu2+,会有一部分Zn与Cu2+直接反应,
高考化学一轮复习 原电池及化学电源练习-人教版高三全册化学试题.doc
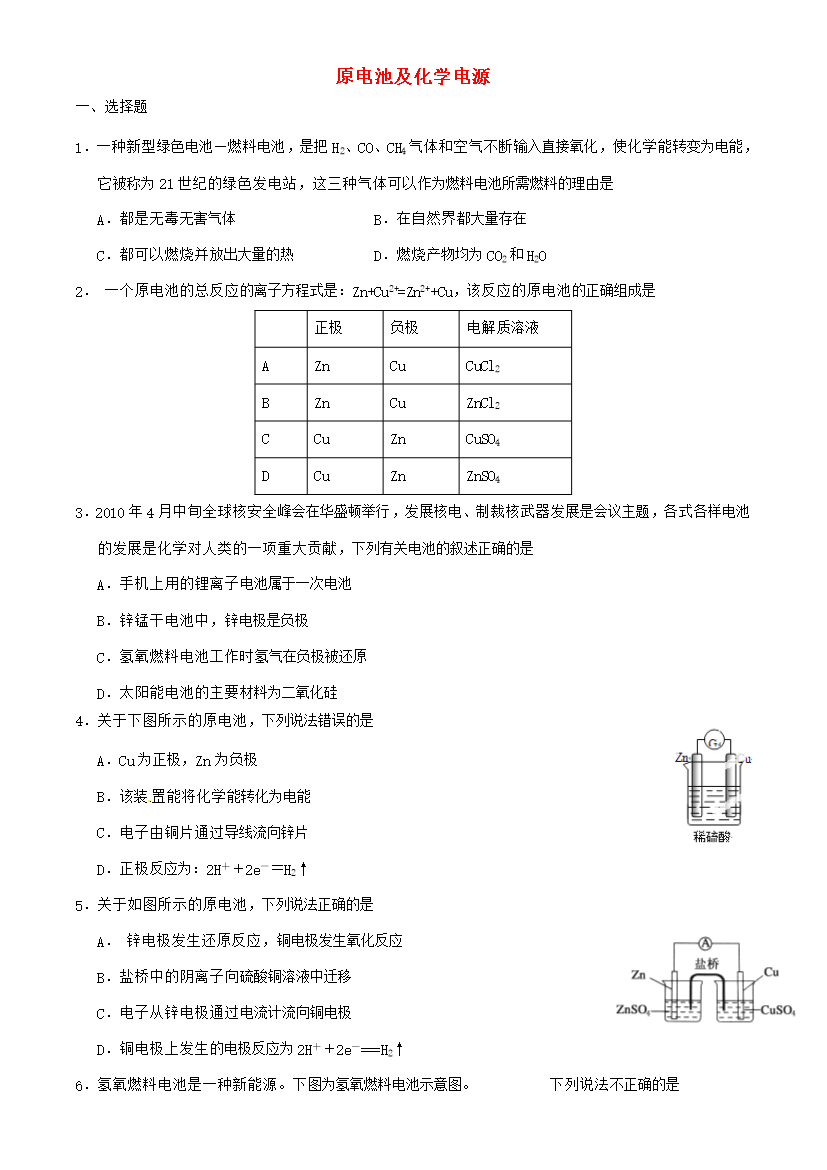
原电池及化学电源选择题1.一种新型绿色电池—燃料电池是把H2、CO、CH4气体和空气不断输入直接氧化使化学能转变为电能它被称为21世纪的绿色发电站这三种气体可以作为燃料电池所需燃料的理由是A.都是无毒无害气体B.在自然界都大量存在C.都可以燃烧并放出大量的热D.燃烧产物均为CO2和H2O2.一个原电池的总反应的离子方程式是:Zn+Cu2+=Zn2++Cu该反应的原电池的正确组成是正极负极电解质溶液AZnCuCuCl2BZnCuZnCl2CCu
