
2009届高考化学试题汇编:中和滴定和PH计算(2).doc

是你****盟主







在线预览结束,喜欢就下载吧,查找使用更方便
相关资料

2009届高考化学试题汇编:中和滴定和PH计算(2).doc
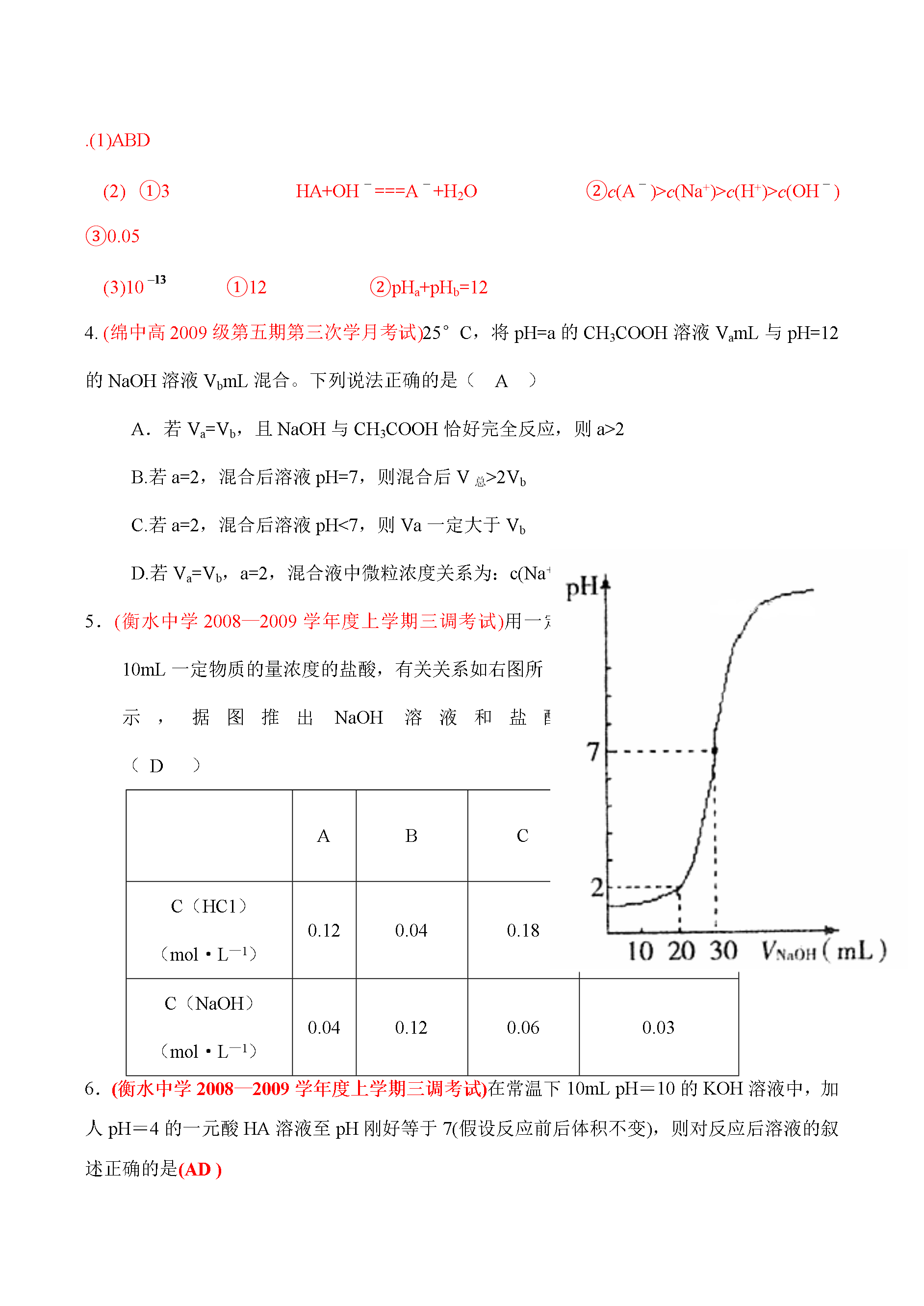
2009届高考化学试题汇编:中和滴定和PH计算(2)1.(武汉一中新疆班09高三年级化学)将pH=1的稀硫酸慢慢加入—定量的BaCl2的溶液中恰好使Ba2+沉淀完全此时溶液的体积为100mL(混合时溶液体积的变化忽略不计)且混合溶液的pH=2则原BaCl2溶液中Cl-的浓度为(A)A.0.011mol/LB.0.22mol/LC.0.022mol/LD.0.11mol/L2.(飞龙中学2009届理科复习班第四次理科综合)(13分)(1)在温度t℃时pH

2009届高考化学试题汇编:中和滴定和PH计算(2).doc
2009届高考化学试题汇编:中和滴定和PH计算(2)1.(武汉一中新疆班09高三年级化学)将pH=1的稀硫酸慢慢加入—定量的BaCl2的溶液中,恰好使Ba2+沉淀完全,此时溶液的体积为100mL(混合时溶液体积的变化忽略不计),且混合溶液的pH=2,则原BaCl2溶液中Cl-的浓度为(A)A.0.011mol/LB.0.22mol/LC.0.022mol/LD.0.11mol/L2.(飞龙中学2009届理科复习班第四次理科综合)(13分)(1)在温度t℃时,pH=3的某水溶液中c(OH-)=10-9mol

2009届高考化学试题汇编:中和滴定和PH计算.doc
2009届高考化学试题汇编:中和滴定和PH计算1.(武汉一中新疆班09高三年级化学)将pH=1的稀硫酸慢慢加入—定量的BaCl2的溶液中,恰好使Ba2+沉淀完全,此时溶液的体积为100mL(混合时溶液体积的变化忽略不计),且混合溶液的pH=2,则原BaCl2溶液中Cl-的浓度为(A)A.0.011mol/LB.0.22mol/LC.0.022mol/LD.0.11mol/L2.(飞龙中学2009届理科复习班第四次理科综合)(13分)(1)在温度t℃时,pH=3的某水溶液中c(OH-)=10-9mol/L,

试题-全国-2009_2009届高考化学试题汇编:中和滴定和PH计算(2).rar
用心爱心专心2009届高考化学试题汇编:中和滴定和PH计算(2)1.(武汉一中新疆班09高三年级化学)将pH=1的稀硫酸慢慢加入—定量的BaCl2的溶液中,恰好使Ba2+沉淀完全,此时溶液的体积为100mL(混合时溶液体积的变化忽略不计),且混合溶液的pH=2,则原BaCl2溶液中Cl-的浓度为(A)A.0.011mol/LB.0.22mol/LC.0.022mol/LD.0.11mol/L2.(飞龙中学2009届理科复习班第四次理科综合)(13分)(1)在温度t℃时,pH=3的某水溶液中c(OH-)=1

试题-全国-2009_2009届高考化学试题汇编:中和滴定和PH计算.rar
用心爱心专心2009届高考化学试题汇编:中和滴定和PH计算1.(辽宁省沈阳二中2008—2009学年上学期高三期中考试)将一定的钠、铝合金置于水中,合金全部溶解,得到20mLpH=14的溶液。然后用1mol/L的盐酸滴定至沉淀量最大时,消耗盐酸40mL。原合金中钠的质量为(A)A.0.92gB.0.69gC.0.46gD.0.23g2.(洛阳一高2008—2009学年高三年级11月月考)25℃时,在20ml0.1mol·L-1NaOH溶液中逐滴加入0.2mol·L-1醋酸溶液,曲线如图所示,有关粒子浓度关
