
2008高考化学化学实验专题复习三(实验设计、评价与综合实验).doc

是翠****ng










亲,该文档总共44页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

2008高考化学化学实验专题复习三(实验设计、评价与综合实验).doc
用心爱心专心115号编辑2008高考化学化学实验专题复习三(实验设计、评价与综合实验)1、下列实验过程中产生的现象与对应的图形相符合的是ANaHSO3粉末加入HNO3溶液中BH2S气体通入氯水中CNaOH溶液滴入Ba(HCO3)2溶液中DCO2气体通入澄清石灰水中2、由K2SO4和Na2SO4组成的混合物mg为测定其中的K2SO4的质量分数将该混合物加入到足量的BaCl2溶液中搅拌充分反应

2008高考化学化学实验专题复习三(实验设计、评价与综合实验).doc
用心爱心专心115号编辑2008高考化学化学实验专题复习三(实验设计、评价与综合实验)1、下列实验过程中产生的现象与对应的图形相符合的是ANaHSO3粉末加入HNO3溶液中BH2S气体通入氯水中CNaOH溶液滴入Ba(HCO3)2溶液中DCO2气体通入澄清石灰水中2、由K2SO4和Na2SO4组成的混合物mg,为测定其中的K2SO4的质量分数,将该混合物加入到足量的BaCl2溶液中,搅拌,充分反应后,过滤出沉淀,不经洗涤就烘干,然后冷却、称重,得沉淀质量Wg,据此计算出K2SO4的质量分数,则结果将A.偏

试题-全国-2008_2008高考化学化学实验专题复习三(实验设计、评价与综合实验).rar
用心爱心专心115号编辑2008高考化学化学实验专题复习三(实验设计、评价与综合实验)1、下列实验过程中产生的现象与对应的图形相符合的是ANaHSO3粉末加入HNO3溶液中BH2S气体通入氯水中CNaOH溶液滴入Ba(HCO3)2溶液中DCO2气体通入澄清石灰水中2、由K2SO4和Na2SO4组成的混合物mg,为测定其中的K2SO4的质量分数,将该混合物加入到足量的BaCl2溶液中,搅拌,充分反应后,过滤出沉淀,不经洗涤就烘干,然后冷却、称重,得沉淀质量Wg,据此计算出K2SO4的质量分数,则结果将A.偏

2008高考化学专题复习17 化学实验设计与评价.doc
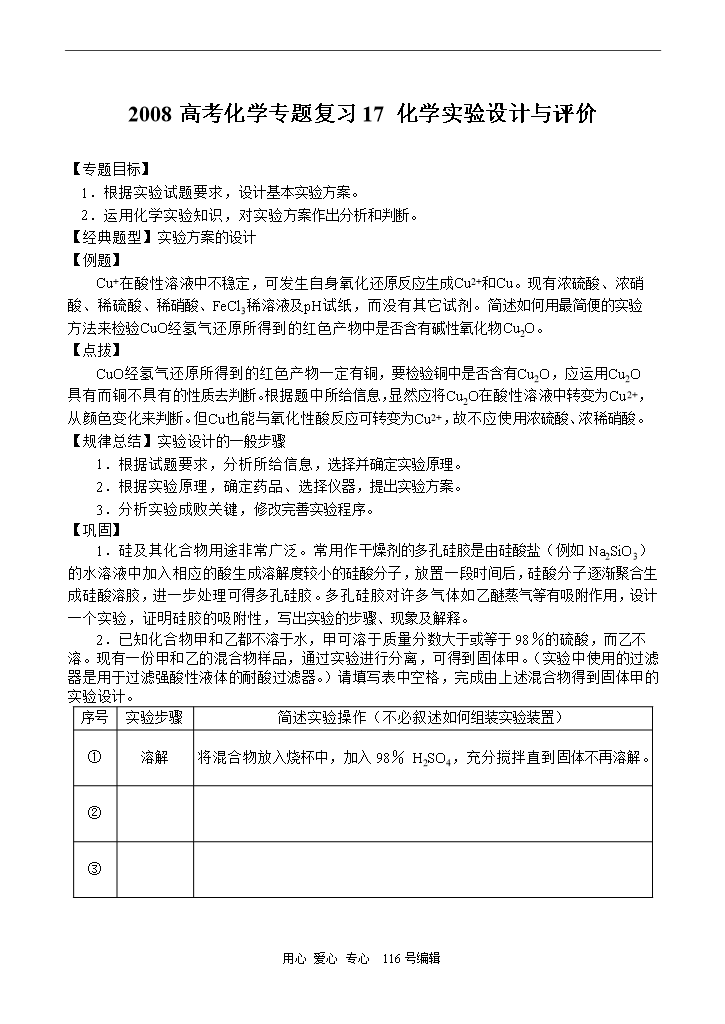
用心爱心专心116号编辑2008高考化学专题复习17化学实验设计与评价【专题目标】1.根据实验试题要求,设计基本实验方案。2.运用化学实验知识,对实验方案作出分析和判断。【经典题型】实验方案的设计【例题】Cu+在酸性溶液中不稳定,可发生自身氧化还原反应生成Cu2+和Cu。现有浓硫酸、浓硝酸、稀硫酸、稀硝酸、FeCl3稀溶液及pH试纸,而没有其它试剂。简述如何用最简便的实验方法来检验CuO经氢气还原所得到的红色产物中是否含有碱性氧化物Cu2O。【点拔】CuO经氢气还原所得到的红色产物一定有铜,要检验铜中是否
2008高考化学专题复习17 化学实验设计与评价.doc
用心爱心专心116号编辑2008高考化学专题复习17化学实验设计与评价【专题目标】1.根据实验试题要求设计基本实验方案。2.运用化学实验知识对实验方案作出分析和判断。【经典题型】实验方案的设计【例题】Cu+在酸性溶液中不稳定可发生自身氧化还原反应生成Cu2+和Cu。现有浓硫酸、浓硝酸、稀硫酸、稀硝酸、FeCl3稀溶液及pH试纸而没有其它试剂。简述如何用最简便的实验方法来检验CuO经氢气还原所得到的红色产物中是否含有碱性氧化物Cu2O。【点拔】CuO经氢气还原所得到的红色产物一定有铜要检验铜中是否
