
一种缩醛键骨架的超支化聚磷酸酯材料及其制备方法与应用.pdf

子安****吖吖









亲,该文档总共17页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

一种缩醛键骨架的超支化聚磷酸酯材料及其制备方法与应用.pdf
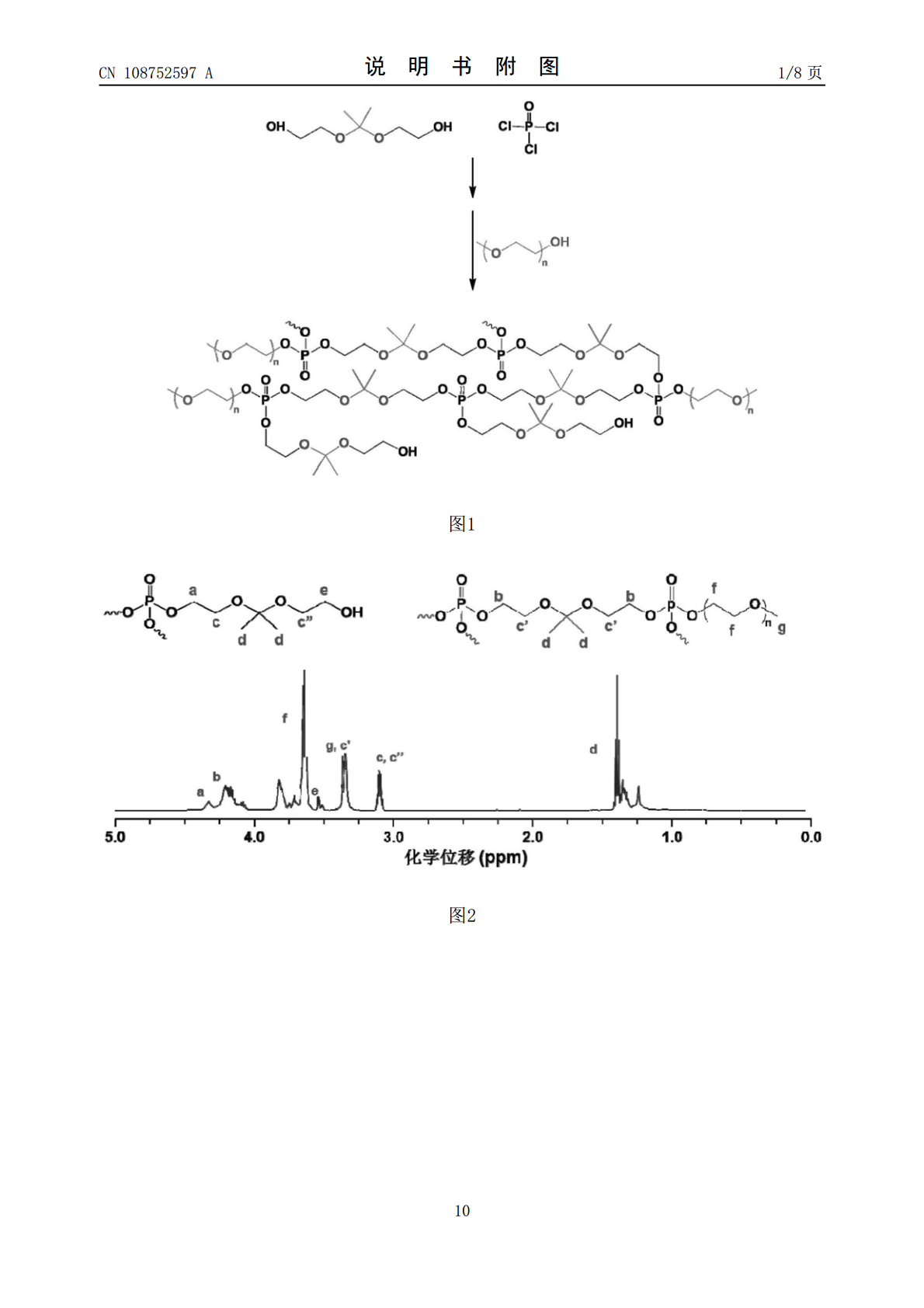
本发明公开了一种缩醛键骨架的超支化聚磷酸酯材料及其制备方法与应用。该方法包括以下步骤:(1)将含有缩醛键的二醇和三乙胺溶于溶剂,再在冰浴下加入三氯氧磷,搅拌反应;(2)反应结束后,加入甲氧基聚乙二醇,搅拌反应,得缩醛键骨架的超支化聚磷酸酯材料。本发明的超支化聚磷酸酯材料具有良好的生物相容性和可降解性。该超支化聚磷酸酯材料自组装形成纳米颗粒,在肿瘤细胞内的内涵体/溶酶体酸性环境中,缩醛键断裂变成两个羟基,使颗粒内核磷酸酯由疏水性向亲水性转变,颗粒崩解,使光敏剂药物快速释放出来,增加肿瘤细胞内游离的光敏剂的浓

超支化聚缩醛的制备及其在药物载体领域的应用.docx
超支化聚缩醛的制备及其在药物载体领域的应用超支化聚缩醛的制备及其在药物载体领域的应用超支化聚缩醛是一种应用极广的高分子材料,可以作为药物或基因载体,有着良好的生物相容性和高载药量等特点。本文将阐述超支化聚缩醛的制备方法及其在药物载体领域的应用。超支化聚缩醛的制备方法超支化聚缩醛是由缩醛单体(trimethylolpropanetriacrylate,TMPTA)在存在三(丙烯腈酸甲酯)嵌段共聚物(P123)的条件下通过自由基聚合制备的。制备方法如下:1.将TMPTA、P123和丙酮混合,加入反应瓶中;2.

超支化聚缩醛的制备及其在药物载体领域的应用的中期报告.docx
超支化聚缩醛的制备及其在药物载体领域的应用的中期报告一、研究背景和意义聚酸酯、聚酯、聚醚等高分子材料一直是药物载体领域的研究热点。这些材料的特别结构和生物相容性可使它们被用于制备各种形式的药物载体,如微球、纳米粒子和纤维等,并广泛应用于药物缓释、靶向、保护和控制释放等方面。然而,现有的聚合物材料还存在一些缺陷,例如生物降解速率慢、腐蚀性大、成本高等问题。为解决这些问题,研究人员不断探索新的聚合物材料。超支化聚缩醛是一种新型的聚合物材料,具有很强的生物相容性、生物可降解性,并且容易制备,是一种良好的药物载体

一种含有硫醚键的超支化聚磷酸酯材料及其制备方法和应用.pdf
一种含有硫醚键的超支化聚磷酸酯材料及其制备方法和应用,其中,制备方法包括以下步骤:(1)将1,2‑乙二硫醇和三烯丙基磷酸酯溶于溶剂,并加入催化剂,搅拌并通氮气除氧,然后在加热下发生A

一种聚缩醛组合物及其制备方法和应用.pdf
本发明提供了一种聚缩醛组合物及其制备方法,所述聚缩醛组合物包括聚缩醛、热塑性聚氨酯弹性体、异氰酸酯相容剂、碳酸酯类脱挥剂。所述聚缩醛组合物的制备方法,包括通过含吡啶环的酯类化合物作为失活/交联剂制备限制粒径范围的主/侧链接入氧化石墨烯的功能化石墨烯接枝聚缩醛树脂原粉,并将该原粉与热塑性聚氨酯弹性体、异氰酸酯相容剂、碳酸酯类脱挥剂反应挤出的步骤。本发明利用功能化氧化石墨烯对支化聚缩醛树脂原粉在特定条件下进行简单修饰,通过将该聚缩醛树脂原粉与热塑性聚氨酯弹性体、异氰酸酯相容剂熔融混炼,辅以碳酸酯类脱挥剂进行脱
