
高中化学 第三章 烃的含氧衍生物 3.1 醇酚 3.1.1 醇导学案 新人教版选修5-新人教版高二选修5化学学案.doc

纪阳****公主








在线预览结束,喜欢就下载吧,查找使用更方便
相关资料

高中化学 第三章 烃的含氧衍生物 3.1 醇酚 3.1.1 醇导学案 新人教版选修5-新人教版高二选修5化学学案.doc
第一节第一课时醇【学习目标】1、掌握乙醇的组成、结构和主要化学性质。2、掌握醇类的取代反应、消去反应和氧化反应的原理。3、了解醇类的结构特征、一般通性和几种典型醇的用途一、乙醇的分子结构分子式;结构式;结构简式;官能团结构简式;官能团的电子式。乙醇的物理性质色、气味、挥发、密度比水、能溶解多种和能与水

高中化学 第三章 烃的含氧衍生物 3.1 醇酚 3.1.1 醇导学案 新人教版选修5-新人教版高二选修5化学学案.doc
第一节第一课时醇【学习目标】1、掌握乙醇的组成、结构和主要化学性质。2、掌握醇类的取代反应、消去反应和氧化反应的原理。3、了解醇类的结构特征、一般通性和几种典型醇的用途一、乙醇的分子结构分子式;结构式;结构简式;官能团结构简式;官能团的电子式。乙醇的物理性质色、气味、挥发、密度比水、能溶解多种和能与水
高中化学 第三章 烃的含氧衍生物 3.1 醇 酚 3.1.1 醇教案 新人教版选修5-新人教版高二选修5化学教案.doc
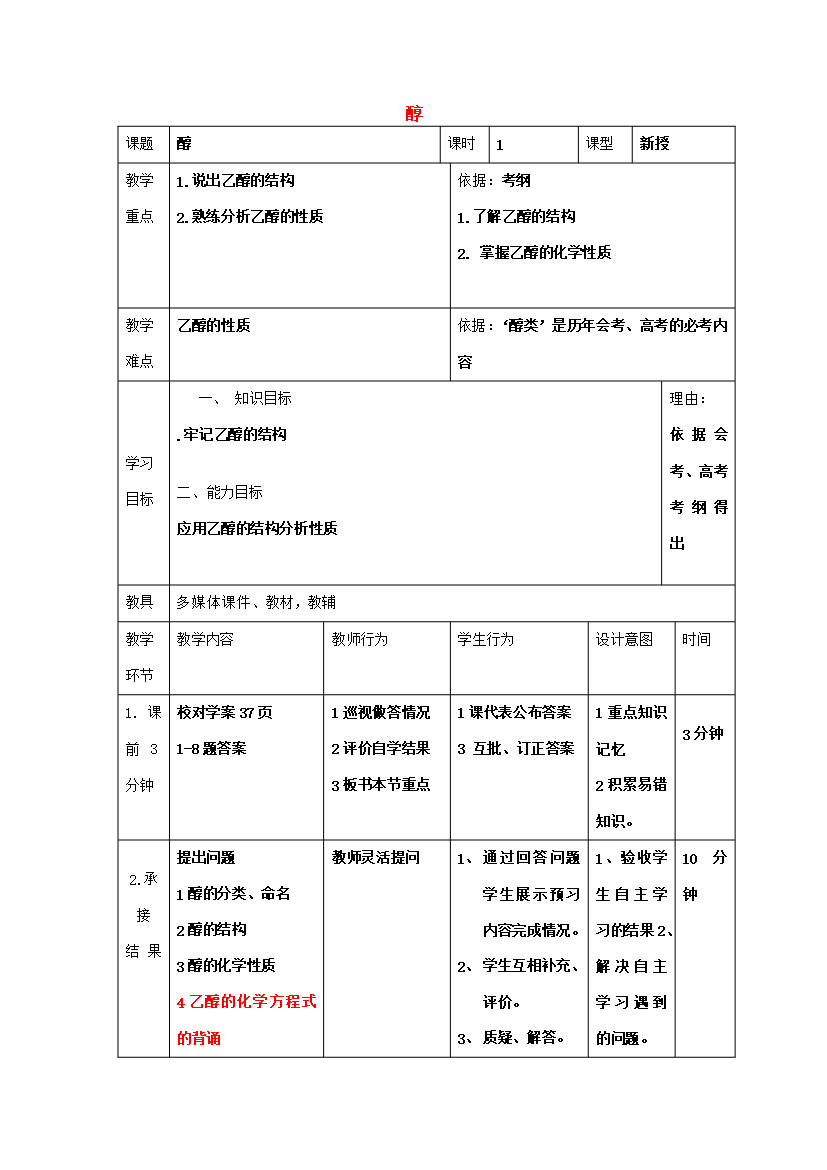
醇课题醇课时1课型新授教学重点1.说出乙醇的结构2.熟练分析乙醇的性质依据:考纲1.了解乙醇的结构2.掌握乙醇的化学性质教学难点乙醇的性质依据:‘醇类’是历年会考、高考的必考内容学习目标知识目标.牢记乙醇的结构二、能力目标应用乙醇的结构分析性质理由:依据会考、高考考纲得出教具多媒体课件、教材教辅教学环节教学内容教师行为学生行为设计意图时间1.课前3分钟校对学案37页1-8题答案1巡视做答情况2评价自学结果3板书本节重点1课代表公布答案3互批、订正答案1重点知识记忆2积累易错知识。3分钟承接结

高中化学 第三章 烃的含氧衍生物 3.1 醇酚 3.1.1 醇课件 新人教版选修5-新人教版高二选修5化学课件.ppt
第一节醇酚酚:乙醇的物理性质下列物质中属于醇属于酚.二、醇分类三、醇的命名CH3—CH2—CH—CH3原因:醇类分子间存在氢键。2CH3CH2OH+2Na→2CH3CH2ONa+H2↑2.消去反应(分子内脱水)⑤为何使液体温度迅速升到170℃不能过高或高低?①放入几片碎瓷片作用是什么?⑥混合液颜色如何变化?为什么?【思考?】3.取代反应4.醇的催化氧化规律4.醇

高中化学 第三章 烃的含氧衍生物 3.1 醇 酚 3.1.2 醇习题课教案 新人教版选修5-新人教版高二选修5化学教案.doc
醇类乙醇课题醇类乙醇课时1课型习题课教学重点1.记牢乙醇的结构和性质2.归纳醇类的结构和性质依据:考纲1.了解醇类的结构2.掌握乙醇的性质教学难点熟练运用醇类的性质依据:‘醇类’是历年会考、高考的必考内容学习目标知识目标1.记牢乙醇的性质二、能力目标1运用醇类的性质理由:依据会考、高考考纲得出教具多媒体课件、教材教辅教学环节教学内容教师行为学生行为设计意图时间1.课前3分钟核对课时作业8答案1巡视做答情况2评价自学结果3板书本节重点1课代表公布答案3互批、订正答案1重点知识记忆2积
