
化学反应的限度省公共课一等奖全国赛课获奖课件.pptx

和蔼****娘子








亲,该文档总共26页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

化学反应的限度省公共课一等奖全国赛课获奖课件.pptx
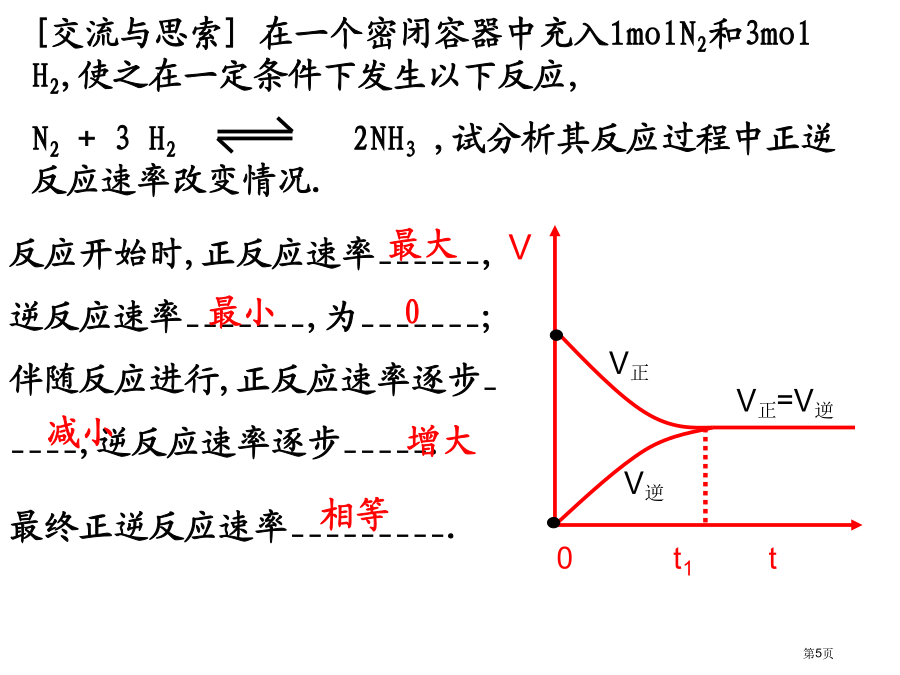
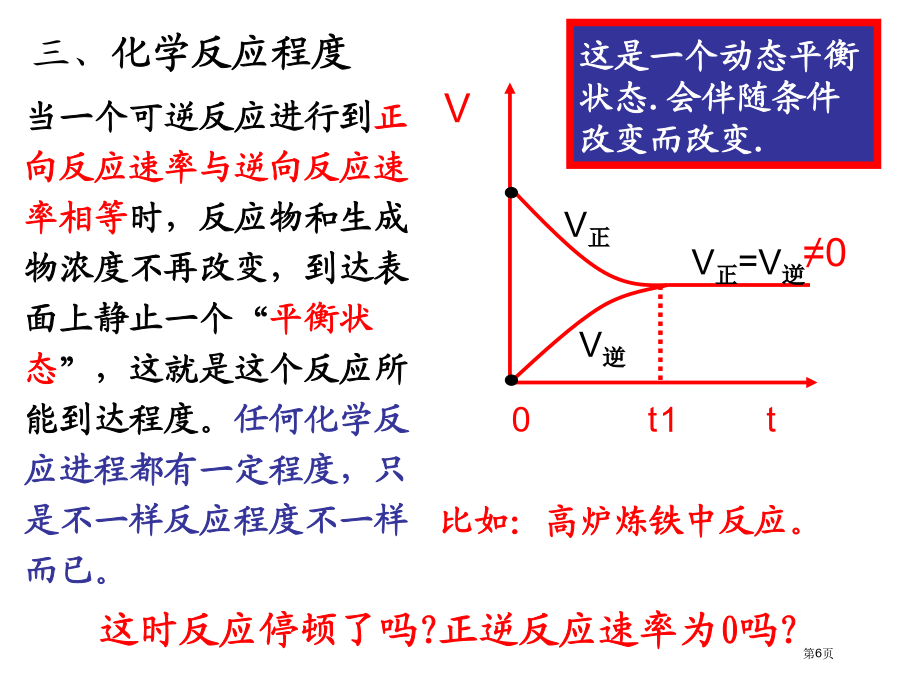
第三节化学反应速率和程度第3课时化学反应程度观察以下各组化学方程式,寻找每组内两个化学反应异同,谈谈你对化学反应认识。三、化学反应程度[复习]举例说明什么是可逆反应?反应开始时,正反应速率______,逆反应速率_______,为_______;伴随反应进行,正反应速率逐步_____,逆反应速率逐步_____.最终正逆反应速率_________.三、化学反应程度三、化学反应程度[思索]怎样了解V(正)=V(逆)?(4)A、B、C分子数比一定为1:3:2吗?[思索]怎样判断一个可逆反应已到达化学平衡状态?(

化学反应的速率和限度省公共课一等奖全国赛课获奖课件.pptx
第三节化学反应速率和限度思索与交流:二、化学反应程度P44可逆反应1、化学平衡状态定义:一定条件下,可逆反应里,正反应速率和逆反应速率相等,反应混合物中各组分浓度保持不变状态三、化学反应条件控制思索与交流:角色扮演演示文稿123后等怎样提升煤燃烧效率?归纳:为何要控制反应条件:练习:1、化学反应速率及其表示方法。2、影响化学反应速率原因。3、化学反应程度和化学平衡状态,以及化学平衡状态特征判断。4、化学反应条件控制。

化学反应的方向速率和限度省公共课一等奖全国赛课获奖课件.pptx
1、自发过程与非自发过程自发过程共同基本特征:高处水(2)自发过程含有作功能力。(3)自发过程有一定程度。2、影响化学反应方向原因不过在现实中有不少吸热过程也是自发过程。在不一样状态下,组成系统微观粒子运动混乱程度不一样熵概念初步热力学第三定律标准摩尔熵(1)物质含微粒越多,结构越复杂,熵值越大。(4)同一物质体积越大,熵值越大。课堂练习:dD+eESm213.669.94228.0205.0NH4Cl(s)=NH3(g)+HCl(g)△rSm=284.94J·mol-1·K-1△rHm=176.9

考查点化学反应速率与反应限度省公共课一等奖全国赛课获奖课件.pptx
考查点13化学反应速率与反应程度一、化学反应速率注意点:同一个反应,用不一样物质来表示反应速率,数值不一定相同,所以应注明是由哪种物质表示。同一反应中,各物质速率之比等于它们在化学方程式中化学计量数之比。1、内因对化学反应速率影响2、外界条件对化学反应速率影响(3)压强(5)其它条件思索:1、氯水中有那些微粒?为何?1、可逆反应(1)定义:在同一条件下,反应既可向正方向进行,同时又可向逆方向进行反应。一、化学反应程度(化学平衡)(1)动:动态平衡练习:练习册65页第3题提升燃烧效率方法(1)使燃料与空气或

化学反应工程课件省公共课一等奖全国赛课获奖课件.pptx
催化反应器安全稳定性分析技术一、问题提出对这类事故原因传统认识用化学反应工程学理论对这类事故原因分析二、化学反应体系多定态特征化学反应体系多定态特征主要性三、CSTR定态及稳定性分析CSTR中发生一级不可逆放热反应多定态特征及定态稳定性CSTR热量衡算CSTR热量衡算CSTR定态解进料温度对CSTR定态影响流量对CSTR定态影响在CSTR反应器中发生吸热反应定态特征CSTR定态稳定判据CSTR瞬态特征分析CSTR瞬态特征分析CSTR瞬态特征分析CSTR瞬态特征分析CSTR瞬态特征分析CSTR瞬态特征分析C
