
选修化学平衡省公共课一等奖全国赛课获奖课件.pptx

人生****奋斗









亲,该文档总共82页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

选修化学平衡省公共课一等奖全国赛课获奖课件.pptx
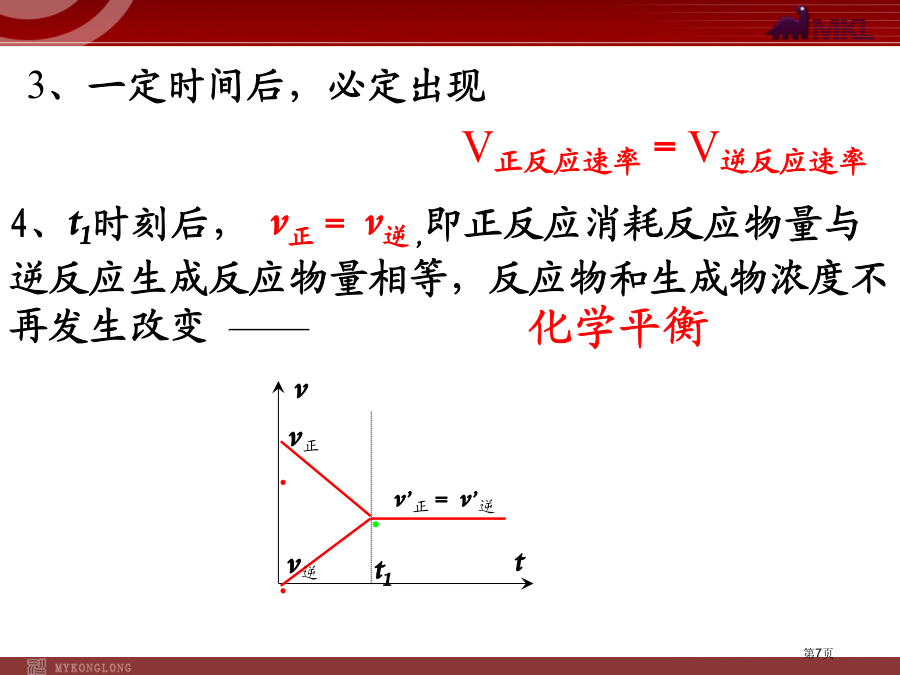
第二章化学反应速率和化学平衡复习:什么叫可逆反应?可逆反应有哪些特点?第三节化学平衡过程分析:讨论:在一定条件下,到达溶解平衡后,蔗糖晶体质量和溶液浓度是否改变?溶解和结晶过程是否停顿?一、化学平衡建立过程3、一定时间后,必定出现二、化学平衡⑴反应条件:注意:平衡时,反应混合物各组成成份物质量浓度、百分含量恒定,但不相等。同时,平衡状态下,反应体系压强恒定、反应混合气体相对分子质量恒定3、化学平衡特征:4、到达化学平衡标志:以反应mA(g)+nB(g)pC(g)为例,到达平衡标志为:例1、一定条件下,反应

选修四化学平衡省公共课一等奖全国赛课获奖课件.pptx
第二章化学反应速率和化学平衡一、可逆反应t1、定义怎样判断可逆反应是否到达平衡状态?a、同一物质V消耗=V生成1、在一定温度下,可逆反应A(g)+3B(g)2C(g)到达平衡标志是()A.C生成速率与C分解速率相等B.单位时间生成nmolA,同时生成3nmolBC.单位时间生成B速率,与生成C速率相等D.单位时间生成nmolA,同时生成2nmolC2、以下说法能够证实反应N2+3H22NH3已达平衡状态是()A.1个N≡N键断裂同时,有3个H-H键形成B.1个N≡N键断裂同时,有3个H-H键断裂C.1个N

化学平衡省公共课一等奖全国赛课获奖课件.pptx
第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡

化学平衡图像省公共课一等奖全国赛课获奖课件.pptx
化学反应速率和化学平衡图象一.化学反应速率图象小结1.物质百分含量——时间曲线mA(g)+nB(g)pC(g)+qD(g)2.转化率——时间曲线01.如图所表示,图中a曲线表示X(g)+Y(g)2Z(g)+W(s)ΔH>0反应过程,若使a曲线变为b曲线,可采取办法是()03.物质产率——时间曲线转化率0小结

化学选修省公共课一等奖全国赛课获奖课件.pptx
第三节分子性质三、氢键及其对物质性质影响极性共价键非极性共价键2、共用电子对是否有偏向或偏离是由什么原因引发呢?练习:指出以下微粒中共价键类型依据电荷分布是否均匀,共价键有极性、非极性之分,以共价键结合分子是否也有极性、非极性之分呢?含有极性键分子一定是极性分子吗?C=O键是极性键,但从分子总体而言CO2是直线型分子,两个C=O键是对称排列,两键极性相互抵消(F合=0),∴整个分子没有极性,电荷分布均匀,是非极性分子判断ABn型分子极性方法:2.依据含键类型和分子空间构型判断:当ABn型分子空间构型是空间
