
化学平衡图像专题超详细版省公共课一等奖全国赛课获奖课件.pptx

和蔼****娘子








亲,该文档总共32页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

化学平衡图像专题超详细版省公共课一等奖全国赛课获奖课件.pptx
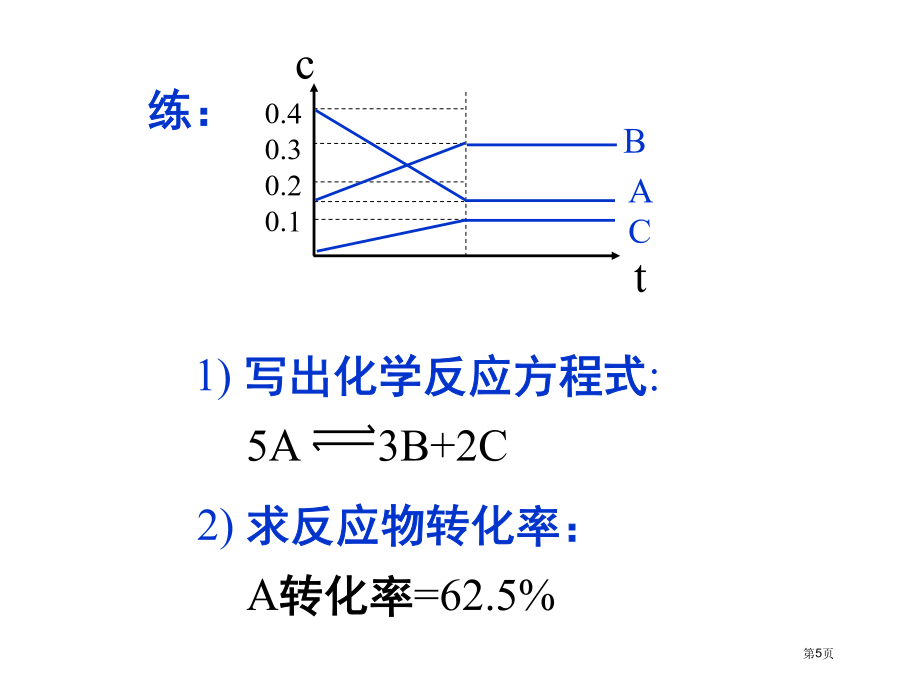
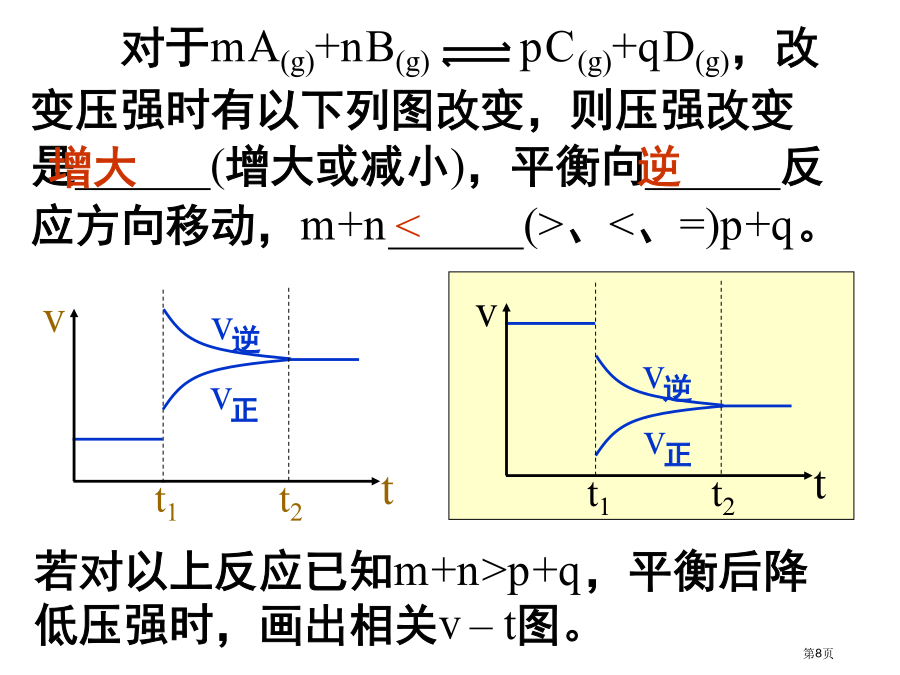
解化学平衡图像题技巧对于化学反应速率和化学平衡相关图象问题,可按以下方法进行分析:①认清坐标系,搞清纵、横坐标所代表意义,并与平衡移动原理(勒夏特列原理)挂钩。②紧紧围绕可逆反应特征,搞清正反应方向是吸还是放热,体积增大还是减小、不变,有没有固体、纯液体物质参加或生成等。③看清速率改变及改变量大小,在条件与改变之间搭桥。④看清起点、拐点、终点,看清曲线改变趋势和图象中线斜率。⑤先拐先平,数值大。比如,在转化率-时间图上,先出现拐点曲线先到达平衡,此时逆向推理可得该改变温高、浓度大、压强高。⑥定一议二。当图

化学平衡图像省公共课一等奖全国赛课获奖课件.pptx
化学反应速率和化学平衡图象一.化学反应速率图象小结1.物质百分含量——时间曲线mA(g)+nB(g)pC(g)+qD(g)2.转化率——时间曲线01.如图所表示,图中a曲线表示X(g)+Y(g)2Z(g)+W(s)ΔH>0反应过程,若使a曲线变为b曲线,可采取办法是()03.物质产率——时间曲线转化率0小结

化学平衡移动图像省公共课一等奖全国赛课获奖课件.pptx
——化学平衡图像题解答相关图象问题,可按以下方法进行分析:①认清坐标系,搞清纵、横坐标所代表意义,并与勒夏特列原理挂钩。②紧紧围绕可逆反应特征,搞清正反应方向是吸还是放热,体积增大还是减小、不变,有没有固体、纯液体物质参加或生成等。③看清速率改变及改变量大小,在条件与改变之间搭桥。④看清起点、拐点、终点,看清曲线改变趋势。⑤先拐先平。比如,在转化率-时间图上,先出现拐点曲线先到达平衡,此时逆向推理可得该改变温度高、浓度大、压强高。⑥定一议二。当图象中有三个量时,先确定一个量不变再讨论另外两个量关系。一、浓

化学平衡省公共课一等奖全国赛课获奖课件.pptx
第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡第三章化学平衡

新概念英语超详细课件省公共课一等奖全国赛课获奖课件.pptx
Lesson25Mrs.Smith'slivingroomMrs.Smith'slivingroomislarge.Translatethefollowingintochinese:platesonthecookercleansome和any使用方法(1)some通惯用于必定句中。Therearesomecigarettesinthebox.(2)any通惯用在否定句中,,或者疑问句中。Therearenotanyspoonsinthecupboard.Arethereanyspoonsinthecupb
