
湖北省八校2017届高三上学期第一次联考(12月)理综化学试题 Word版含解析.doc

一吃****昕靓




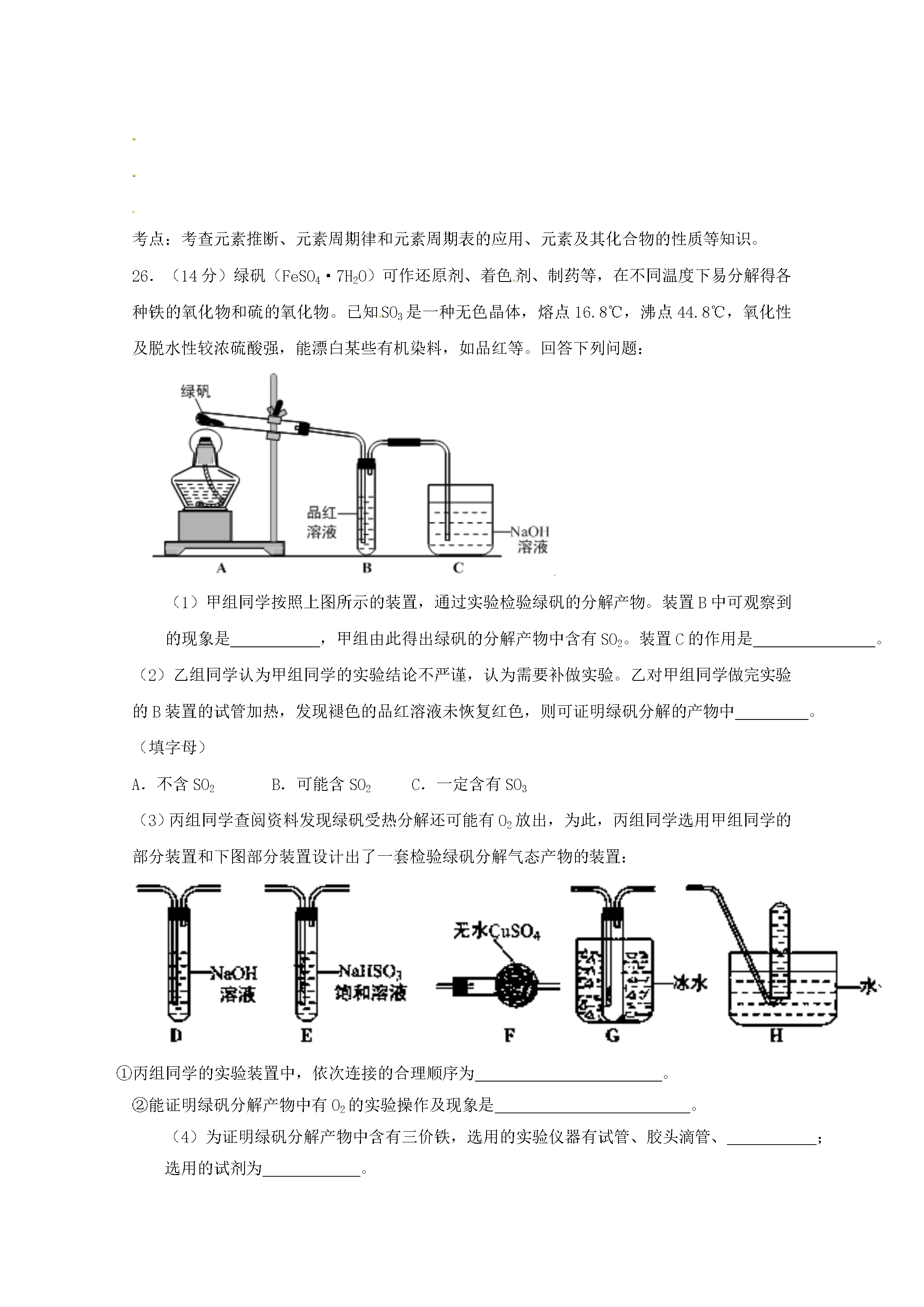


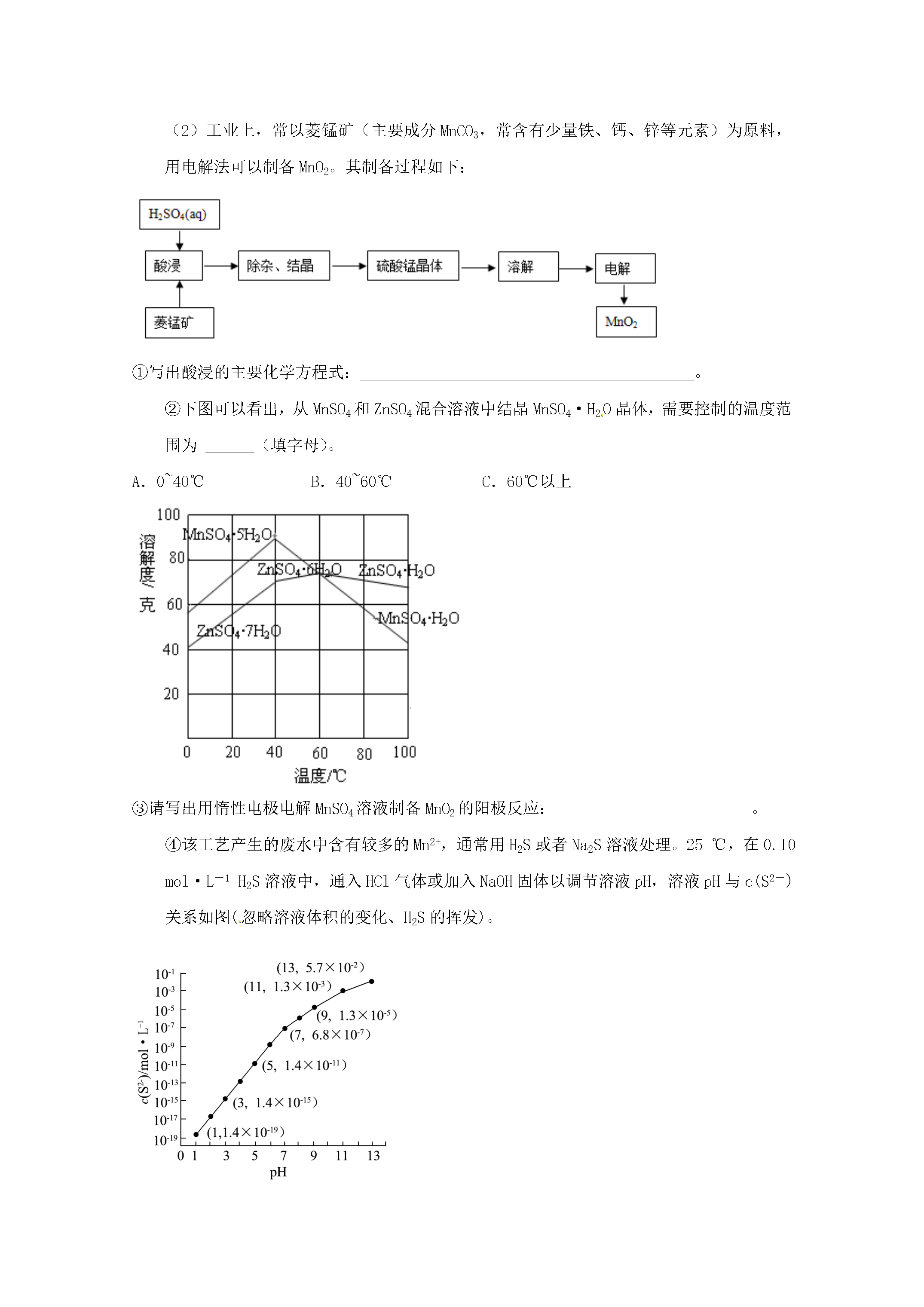

在线预览结束,喜欢就下载吧,查找使用更方便
相关资料

湖北省八校2017届高三上学期第一次联考(12月)理综化学试题 Word版含解析.doc
7.化学与人类的生活息息相关,下列有关说法正确的是()A.因铝表面能形成致密的氧化膜,所以铝制餐具可以长期使用B.因废弃物易污染环境,腈纶不宜大量取代棉、麻等天然材料C.SiO2用途广泛,因其高熔点的特性成为光导纤维的主要原料D.有机玻璃(聚甲基丙烯酸甲酯)是通过缩聚反应制得的【答案】B【解析】试题分析:A、Al对人体是有害的,不能长期使用,故错误;B、棉麻成分是纤维素,容易降解,不易造成环境污染,故正确;C、SiO2不是利用其熔点高的特点,故错误;D、根据有机玻璃的名称,应是发生

湖北省八校2016届高三第一次联考(12月)理综化学试题 WORD版含解析.doc
八校湖北省鄂南高中华师一附中黄石二中荆州中学襄阳四中襄阳五中孝感高中黄冈中学命题学校:湖北襄阳四中命题人:杨立涛杨国明张华任建新侯连峰王朝明审题人:张再良汪响林屈泽兵张旭黄志鹏李神兵考试时间:2015年12月8日上午9:00—11:30全卷满分300分。考试时间150分钟。★祝考试顺利★第Ⅰ卷(选择题共126分)可能用到的相对原子量:H:1N:14O:16S:32Fe:56Cu:64Al:27Zn:65一、选择题:本大题共13小题,每小题6分。在每小题给出的四个选项中,只有一项是符合题目要求的。7.如何解

2023届江西省新八校高三上学期第一次联考理综生物试题 WORD版含解析.docx
江西省景德镇二中上饶中学上栗中学新建二中新八校东乡一中都昌一中丰城中学赣州中学2023届高三第一次联考理科综合试题一、选择题1.下列与化合物存在形式有关的说法错误的是()A.细胞中大多数无机盐以化合物的形式存在B.组成细胞的元素大多以化合物的形式存在C.生物体内的糖类绝大多数以多糖的形式存在D.细胞中绝大部分的水以游离的形式存在2.将某种植物的成熟细胞放入一定浓度的物质A溶液中,发现其原生质体(即植物细胞中细胞壁以内的部分)的体积变化趋势如图所示。下列叙述正确的是()A.0-4h内原生质体体积变化主要因为

广东省东莞市六校2016届高三上学期联考理综化学试题 WORD版含解析.doc
本试卷分为选择题和非选择题两部分,,满分300分,考试时间150分钟。可能用到的相对原子质量:H:1He:4C:12N:14O:16Cl:35.5Na:23S:32Al:27Si:28注意事项:1.考生必须将自己的姓名、统考考号、座位号、考试科目用铅笔涂写在答题卡上。2.选择题共21小题,每小题选出答案后,用铅笔把答题卡上对应的答案标号涂黑。主观题则用黑色钢笔按各题要求答在主观题答题卡相应的位置上。第一部分选择题(共126分)一、选择题(每小题只有一个正确选项,共13小题,每小题6分,共78分)7.化学与

广东省东莞市六校2016届高三上学期联考理综化学试题 Word版含解析.doc
本试卷分为选择题和非选择题两部分,,满分300分,考试时间150分钟。可能用到的相对原子质量:H:1He:4C:12N:14O:16Cl:35.5Na:23S:32Al:27Si:28注意事项:1.考生必须将自己的姓名、统考考号、座位号、考试科目用铅笔涂写在答题卡上。2.选择题共21小题,每小题选出答案后,用铅笔把答题卡上对应的答案标号涂黑。主观题则用黑色钢笔按各题要求答在主观题答题卡相应的位置上。第一部分选择题(共126分)一、选择题(每小题只有一个正确选项,共13小题,
