
(通用版)2020高考化学二轮复习 题型三 化学反应原理综合题的研究大题突破课件.pptx

萌运****魔王







亲,该文档总共61页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

(通用版)2020高考化学二轮复习 题型三 化学反应原理综合题的研究大题突破课件.pptx
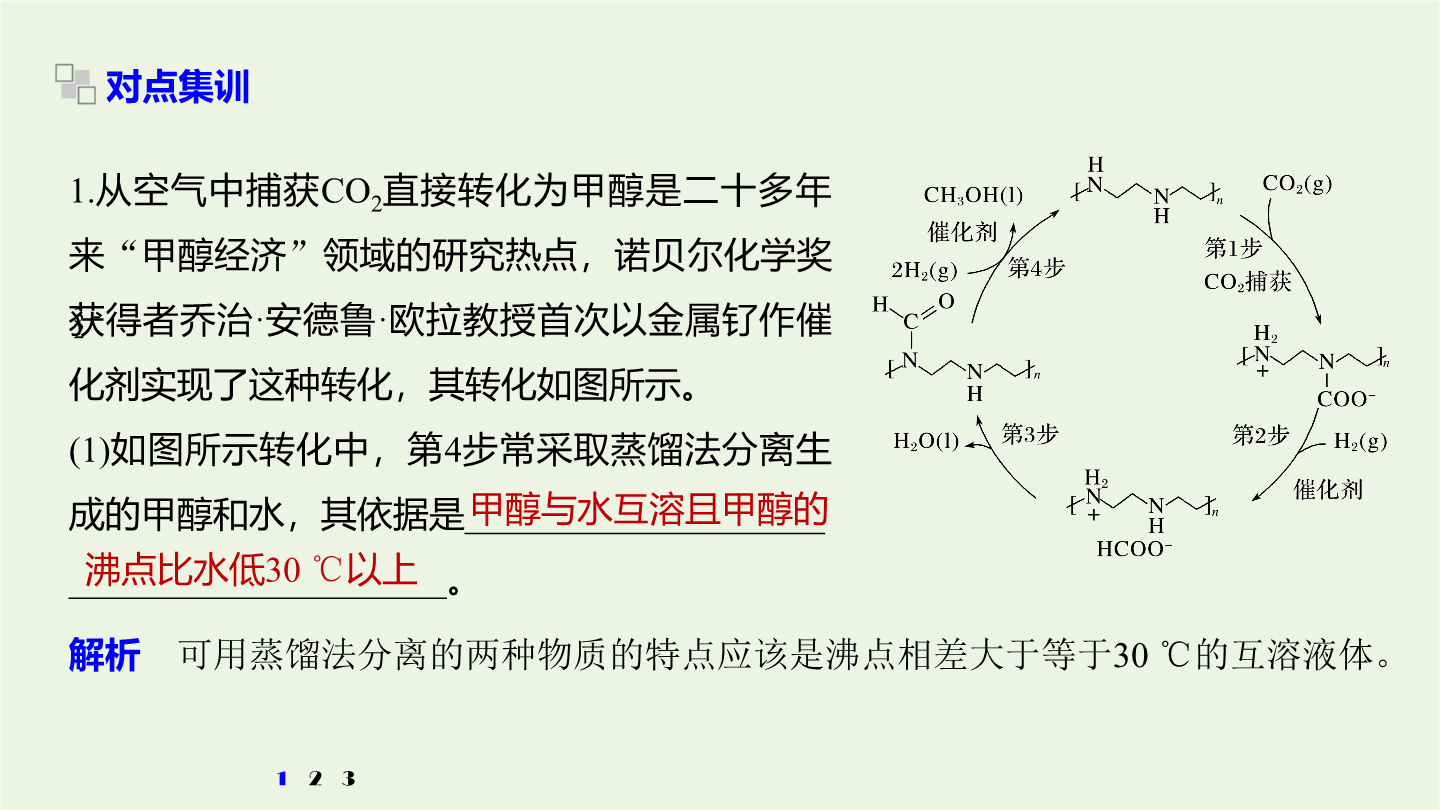
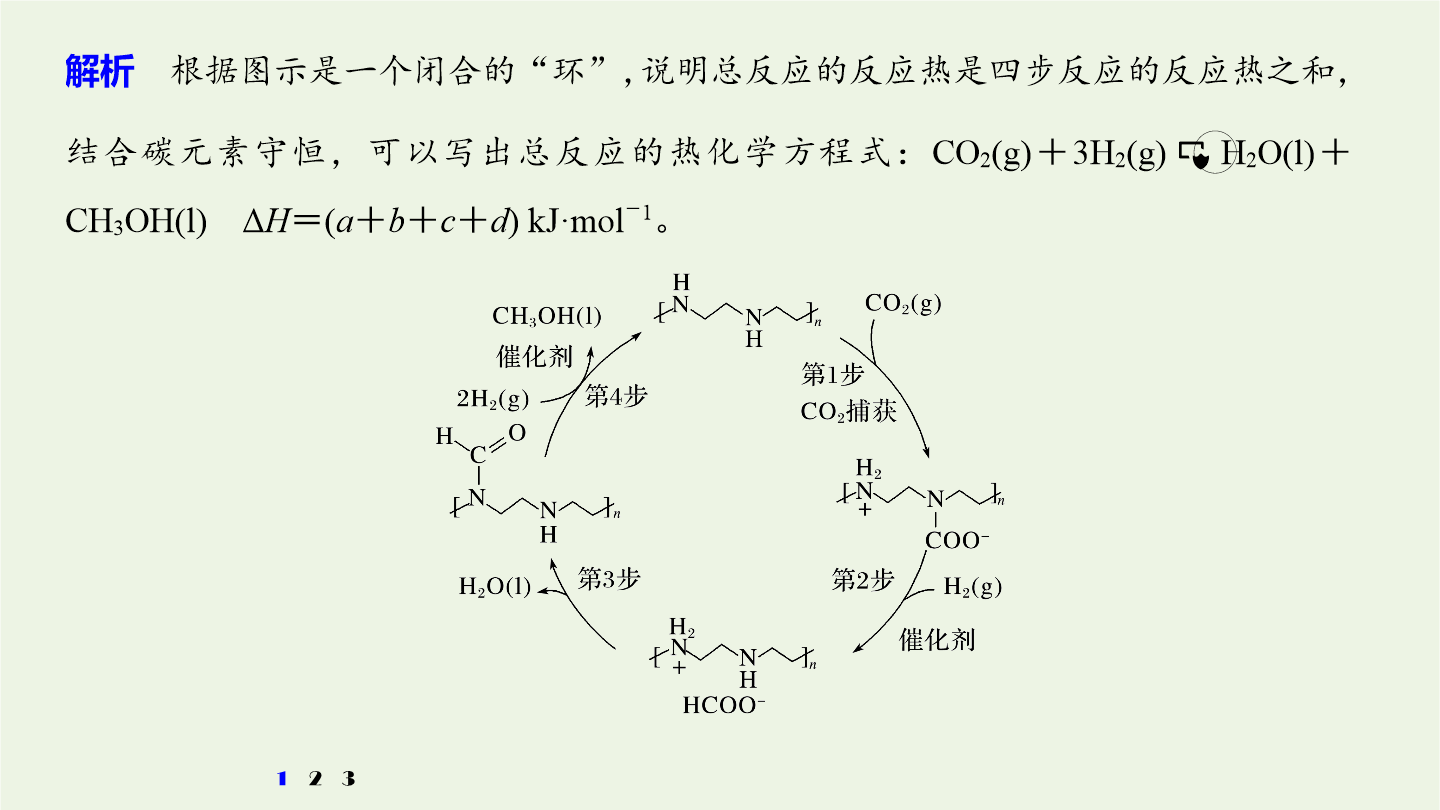
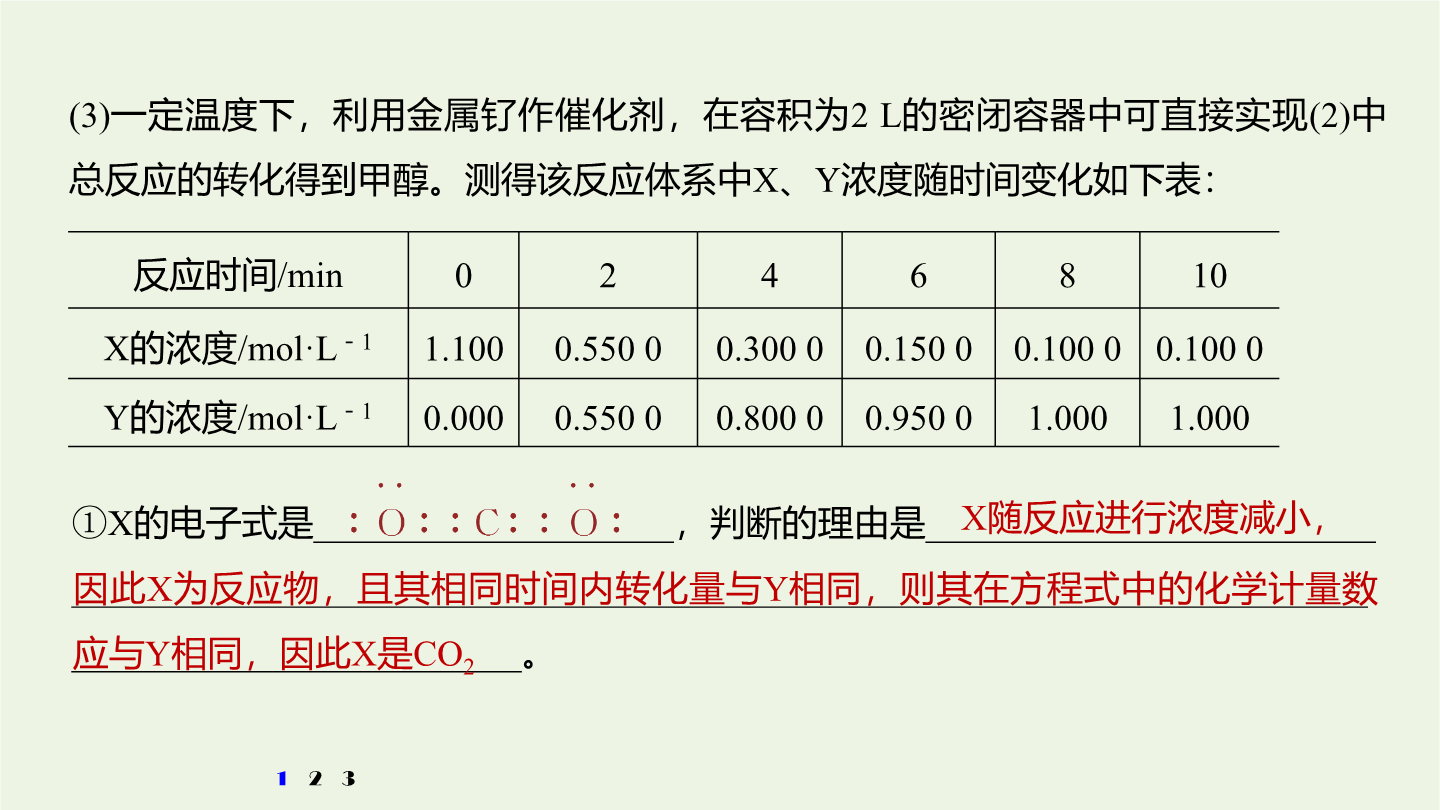
3大题突破整合“精品组件”考向突破一化学平衡与能量变化的结合考向突破一化学平衡与能量变化的结合1.题型特点这类试题往往以化学反应速率,化学平衡知识为主题,借助图像、图表的手段,综合考查关联知识,关联知识主要有:(1)ΔH符号的判断、热化学方程式的书写、应用盖斯定律计算ΔH。(2)化学反应速率的计算与比较,外因对化学反应速率的影响(浓度、压强、温度、催化剂)。(3)平衡常数、转化率的计算,温度对平衡常数的影响;化学平衡状态的判断,用化学平衡的影响因素进行分析和解释。(4)在多层次曲线图中反映化学反应速率、化

课件-全国-2019_(通用版)2020高考化学二轮复习 题型三 化学反应原理综合题的研究大题突破课件.pptx
3大题突破整合“精品组件”考向突破一化学平衡与能量变化的结合考向突破一化学平衡与能量变化的结合1.题型特点这类试题往往以化学反应速率,化学平衡知识为主题,借助图像、图表的手段,综合考查关联知识,关联知识主要有:(1)ΔH符号的判断、热化学方程式的书写、应用盖斯定律计算ΔH。(2)化学反应速率的计算与比较,外因对化学反应速率的影响(浓度、压强、温度、催化剂)。(3)平衡常数、转化率的计算,温度对平衡常数的影响;化学平衡状态的判断,用化学平衡的影响因素进行分析和解释。(4)在多层次曲线图中反映化学反应速率、化

(通用版)2020高考化学二轮复习 题型三 化学反应原理综合题的研究逐空突破课件.pptx
2逐空突破打造“精品组件”常考题空1热化学方程式及反应热的计算常考题空1热化学方程式及反应热的计算1.书写热化学方程式的“五环节”2.利用盖斯定律书写热化学方程式的步骤和方法(1)步骤(2)方法题组一热化学方程式的书写1.依据反应事实书写有关热化学方程式:(1)[2017·天津,7(3)]0.1molCl2与焦炭、TiO2完全反应,生成一种还原性气体和一种易水解成TiO2·xH2O的液态化合物,放热4.28kJ,该反应的热化学方程式为____________________________________

(通用版)2020高考化学二轮复习 题型一 化学实验综合题的研究大题突破课件.pptx
3大题突破整合“精品组件”考向突破一以物质制备为载体的综合实验题考向突破一以物质制备为载体的综合实验题1.无机物制备题的常考方向2.有气体参与的制备实验的注意事项(1)操作顺序问题与气体有关的实验操作顺序:装置选择与连接→气密性检查→装入固体药品→加液体药品→按程序实验→拆卸仪器。(2)加热操作的要求①使用可燃性气体(如H2、CO、CH4等),先用原料气赶走系统内的空气,再点燃酒精灯加热,以防止爆炸。②制备一些易与空气中的成分发生反应的物质(如H2还原CuO的实验),反应结束时,应先熄灭酒精灯,继续通原料

2020版高考化学二轮复习 大题突破一 化学反应原理综合课件.ppt
