
(江苏专用版)2020版高考化学总复习 专题六 第3讲 影响化学平衡的因素 化学平衡的移动课件.pptx

猫巷****晓容









亲,该文档总共86页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

(江苏专用版)2020版高考化学总复习 专题六 第3讲 影响化学平衡的因素 化学平衡的移动课件.pptx
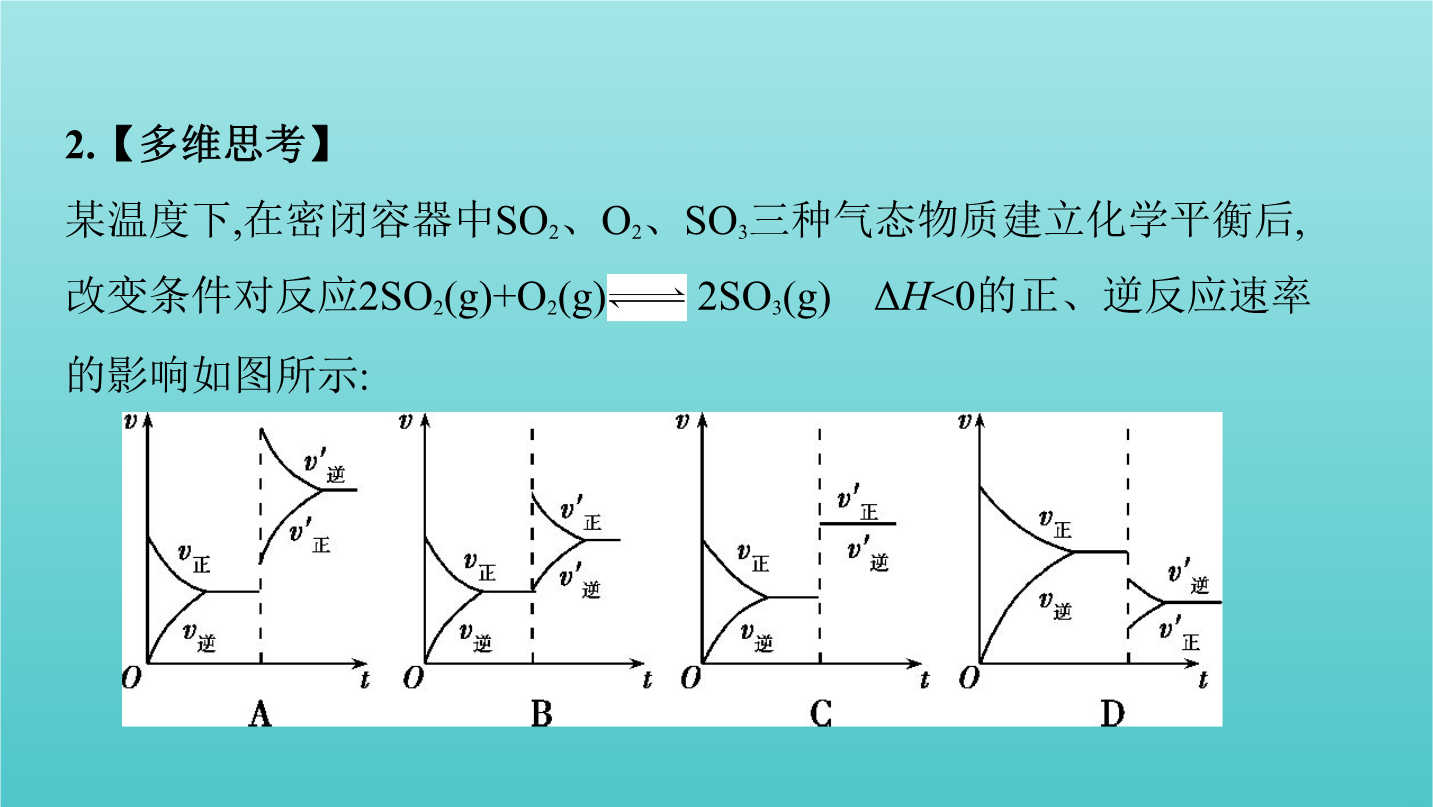
第3讲影响化学平衡的因素化学平衡的移动考点一影响化学平衡移动的因素考点一影响化学平衡移动的因素2.外界因素对化学平衡移动的影响3.勒夏特列原理如果改变影响化学平衡的条件之一(如温度、压强、以及参加反应的化学物质的浓度),平衡将向着能够 减弱这种改变的方向移动。 特别提醒几种特殊情况说明(1)改变固体或纯液体的量,对化学平衡无影响。(2)“惰性气体”对化学平衡的影响。(3)同等程度地改变反应混合物中各物质的浓度时,应视为压强的影响。1.【易错辨析】判断正误,正确的画“√”,错误的画“✕”。(1)工业合成氨反

课件-全国-2019_(江苏专用版)2020版高考化学总复习 专题六 第3讲 影响化学平衡的因素 化学平衡的移动课件.pptx
第3讲影响化学平衡的因素化学平衡的移动考点一影响化学平衡移动的因素考点一影响化学平衡移动的因素2.外界因素对化学平衡移动的影响3.勒夏特列原理如果改变影响化学平衡的条件之一(如温度、压强、以及参加反应的化学物质的浓度),平衡将向着能够 减弱这种改变的方向移动。 特别提醒几种特殊情况说明(1)改变固体或纯液体的量,对化学平衡无影响。(2)“惰性气体”对化学平衡的影响。(3)同等程度地改变反应混合物中各物质的浓度时,应视为压强的影响。1.【易错辨析】判断正误,正确的画“√”,错误的画“✕”。(1)工业合成氨反

(江苏专用版)高考化学总复习 专题六 第3讲 影响化学平衡的因素 化学平衡的移动课件-人教版高三全册化学课件.pptx
第3讲影响化学平衡的因素化学平衡的移动考点一影响化学平衡移动的因素考点一影响化学平衡移动的因素2.外界因素对化学平衡移动的影响3.勒夏特列原理如果改变影响化学平衡的条件之一(如温度、压强、以及参加反应的化学物质的浓度)平衡将向着能够 减弱这种改变的方向移动。 特别提醒几种特殊情况说明(1)改变固体或纯液体的量对化学平衡无影响。(2)“惰性气体”对化学平衡的影响。(3)同等程度地改变反应混合物中各物质的浓度时应视为压强的影响。1.【易错辨析】判断正误正确的画“√”错误的画“✕”。(1)工

2020版高考化学(江苏专用版)新攻略总复习练习:专题六-第3讲 影响化学平衡的因素 化学平衡的移动 WORD版含解析.docx
第3讲影响化学平衡的因素化学平衡的移动一、单项选择题1.CO和NO都是汽车尾气中的有害物质,它们之间能缓慢地发生如下反应:2NO(g)+2CO(g)N2(g)+2CO2(g)ΔH<0,现利用此反应,拟设计一种环保装置,用来消除汽车尾气对大气的污染,下列设计方案可以提高尾气处理效率的是()①选用适当的催化剂②提高装置温度③降低装置的压强④装置中放入碱石灰A.①③B.②④C.①④D.②③答案C选用适当催化剂虽不能提高反应物的转化率,但能加快反应速率,①正确;因为该反应的正反应为放热反应,所以升高温度,平衡向逆

(江苏专用版)高考化学总复习 专题六 第3讲 影响化学平衡的因素 化学平衡的移动练习(含解析)-人教版高三全册化学试题.docx
第3讲影响化学平衡的因素化学平衡的移动一、单项选择题1.CO和NO都是汽车尾气中的有害物质它们之间能缓慢地发生如下反应:2NO(g)+2CO(g)N2(g)+2CO2(g)ΔH<0现利用此反应拟设计一种环保装置用来消除汽车尾气对大气的污染下列设计方案可以提高尾气处理效率的是()①选用适当的催化剂②提高装置温度③降低装置的压强④装置中放入碱石灰A.①③B.②④C.①④D.②③答案C选用适当催化剂虽不能提高反应物的转化率但能加快反应速率①正确;因
